文件名称 培养基模拟灌装(小容量注射剂)无菌生产工艺验证方案 文件编码 页码数 第1页/共20页 颁发部门 品质管理部 执行日期 审 批 部门 姓名 签名 日期 起草人 品质管理部 起草人 生产技术部 起草人 针剂车间 审核人 针剂车间 审核人 生产技术部 审核人 质检中心 审核人 品质管理部 批准人 质量负责人 分发部门: 培养基模拟灌装(小容量注射剂)无菌生产工艺验证小组 文件名称 培养基模拟灌装(小容量注射剂)无菌生产工艺验证方案 文件编码 页码数 第2页/共20页 颁发部门 品质管理部 执行日期 一、概述 厂区无菌操作生产线,按2010版GMP及其附录要求进行设计,是专用于小容量注射剂非最终灭菌产品生产使用
某某产品因无法进行F0≥8分钟湿热灭菌,以达到SAL≤10-6,但处方可以通过微生物滞留过滤器过滤,故采用除菌过滤和无菌工艺相结合的灭菌方法
无菌生产工艺是制药领域中最难的工艺之一,确保产品无菌是该工艺最大的难点,减少无菌工艺药品污染风险的两项重要措施为:①人员的培训 ②无菌工艺验证
按SFDA 化学药品注射剂基本技术要求:培养基灌装验证是对设备、环境以及人员操作的一种系统验证,是判断无菌保证水平的关键手段
故在正式生产前必须按某某产品生产工艺进行培养基模拟灌装验证
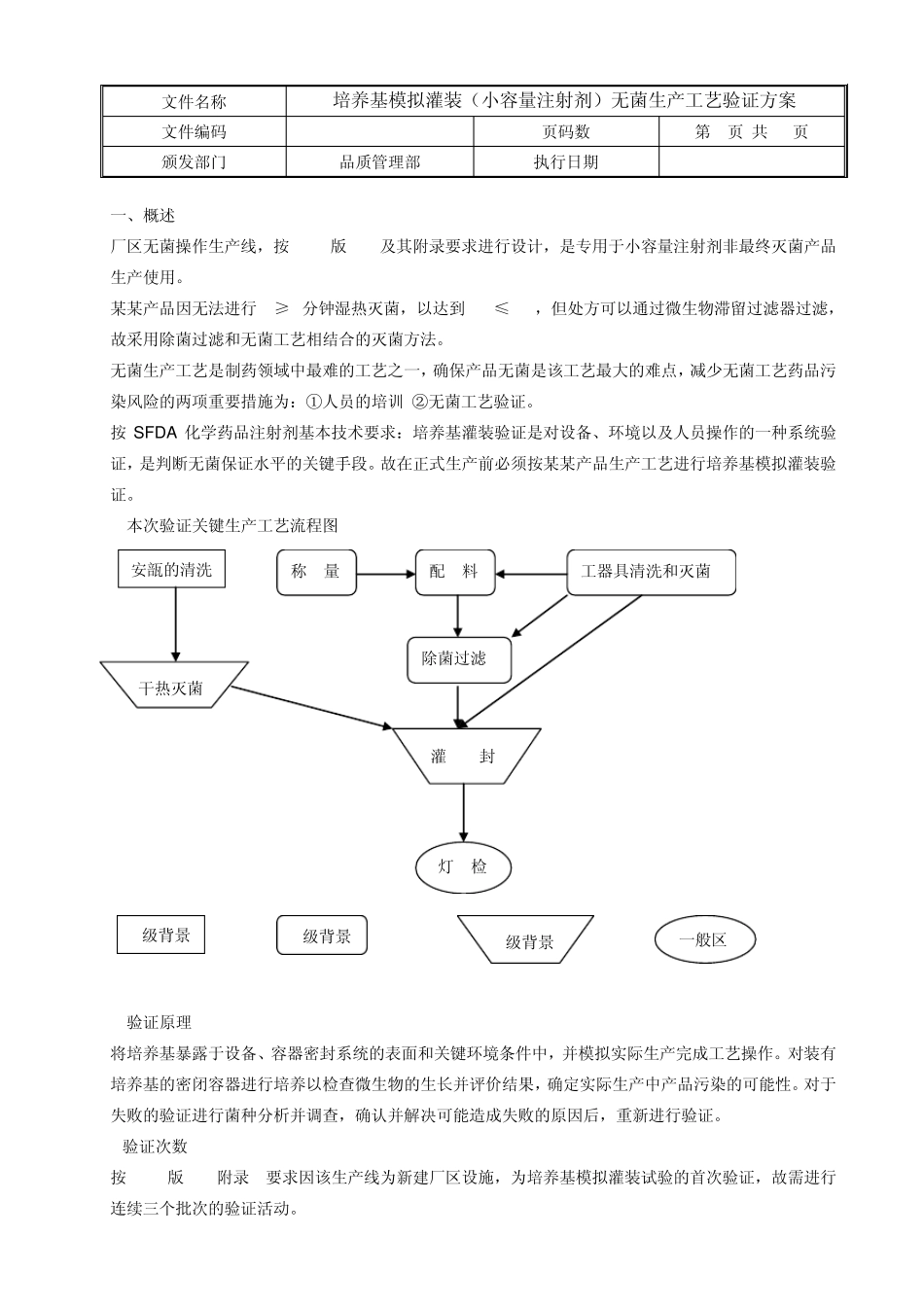
1 本次验证关键生产工艺流程图 2 验证原理 将培养基暴露于设备、容器密封系统的表面和关键环境条件中,并模拟实际生产完成工艺操作
对装有培养基的密闭容器进行培养以检查微生物的生长并评价结果,确定实际生产中产品污染的可能性
对于失败的验证进行菌种分析并调查,确认并解决可能造成失败的原因后,重新进行验证
3验证次数 按2010版GMP附录1要求因该生产线为新建厂区设施,为培养基模拟灌装试验的首次验证,故需进行连续三个批次的验证活动
D级背景 C级背景 安瓿的清洗 干热灭菌 工器具清洗和灭菌