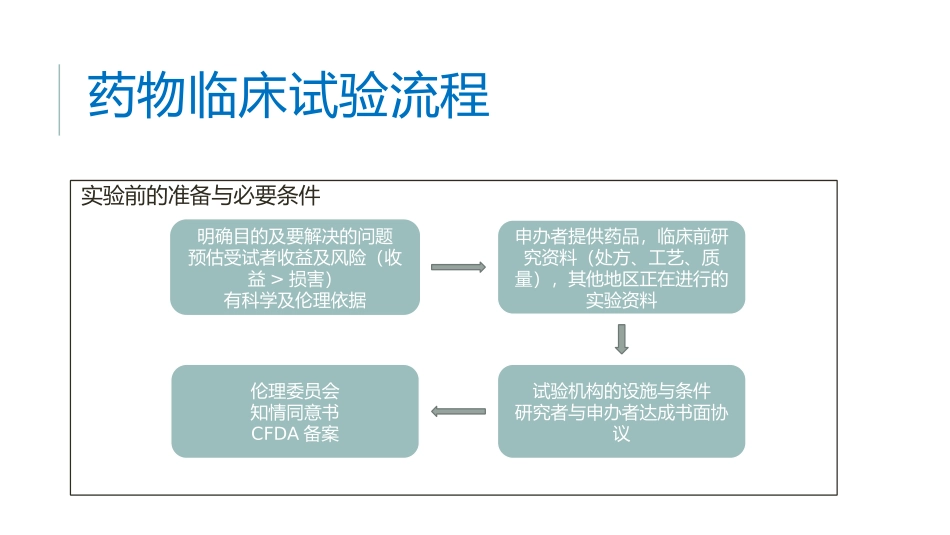
药物临床试验流程药物临床试验流程实验前的准备与必要条件明确目的及要解决的问题预估受试者收益及风险(收益>损害)有科学及伦理依据申办者提供药品,临床前研究资料(处方、工艺、质量),其他地区正在进行的实验资料试验机构的设施与条件研究者与申办者达成书面协议伦理委员会知情同意书CFDA备案试验流程选择试验机构和研究人员建立伦理委员会和质控监督体系制定试验方案签署知情同意书建立SOP(标准操作规程)统计分析、数据处理试验方案GCP对试验方案的要求:1、试验方案由研究者与申办者共同商定并签字;2、试验方案的内容也有相应的条款要求;3、试验各个阶段都要有生物统计学专业人员参与;4、试验方案必须报伦理委员会审批后才可以实施
实验设计的基本原则1、《赫尔辛基宣言》(2000)2、我国《药物临床试验管理规范》(GCP)(2003)3、我国《新药临床研究指导原则》4、《中华人民共和国药品管理法》(2002)5、我国《药物注册管理办法》(2002)6、WHO的GCP指导原则(1993)7、ICH-GCP指导原则(1997)实验设计的基本要求1、代表性:受试者具有该患病人群的共同特征2、合理性:立题的依据、假说的建立应具有科学性3、重复性:在同意条件下临床试验的重现程度4、随机性:“同等可能性”原则分配,样本必须为随机样本5、充分了解临床前研究结果、药政部门审查意见,制定有针对性、完善的方案6、符合伦理道德、科学性原则和统计学要求临床试验方案的内容一、试验题目1、要求:能体现该临床试验的的试验药和对照药名称、治疗病症、设计类型、临床试验的分期和研究目的2、格式:“XX药与XX药对照治疗XX病症的有效性和安全性的随机、双盲、多中心XX期临床试验方案”临床试验方案的内容二、试验目的,试验背景,临床前研究中有临床意义的发现和与该试验有关的临床试验结果、已知对人体的可能危险与受益,及试验药物存在人种差异的可