高中化学学习材料(灿若寒星 **整理制作)2011-2012 学年苏教版化学必修1 同步练习期中复习(一)一、教学内容期中复习二、考点清单1、掌握化学物质的分类方法,理解单质、氧化物、酸、碱、盐等物质之间的相互转化关系2、学会物质的量、摩尔质量、气体摩尔体积、物质的量浓度、质量之间的简单计算3、了解胶体的重要性质和应用4、初步学会过滤、结晶和分液、蒸馏等分离物质的实验技能5、学会 Cl-、SO42-、CO 32-、NH 4+等离子检验的实验技能,掌握焰色反应检验Na、K 元素的实验方法6、初步学会配制一定物质的量浓度的溶液的方法7、了解原子的构成及1— 20 号元素的核外电子排布8、了解从海水中提取Cl 2、 Br 2、I 2 的基本原理和方法,知道Cl 2、Br 2、I 2 的性质及其差异
9、了解氧化还原反应的本质,能简单分析氧化剂和还原剂,标出电子转移的方向和数目
三、全面突破知识点 1:物质的分类与转化:1
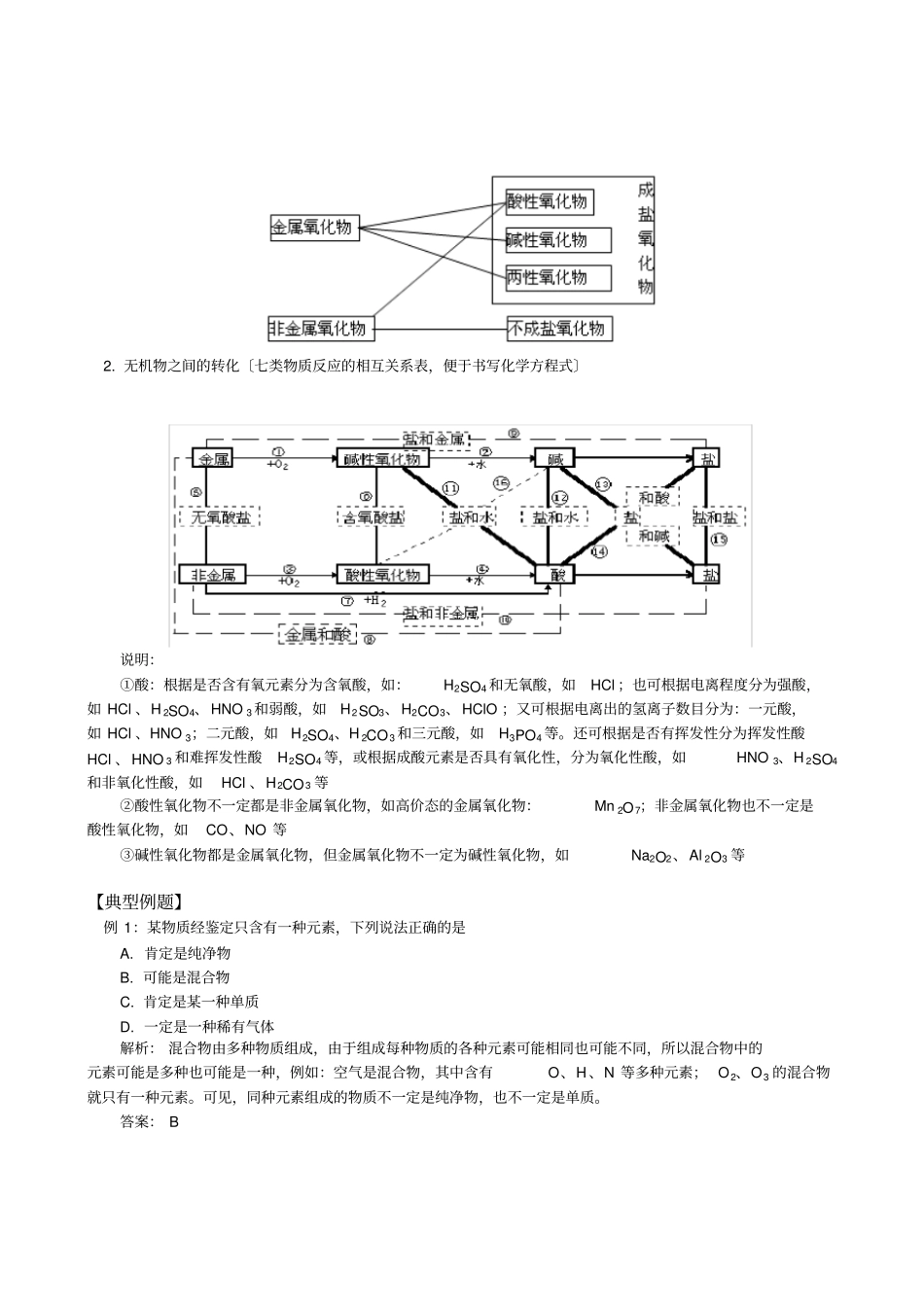
根据物质的组成将物质分类2
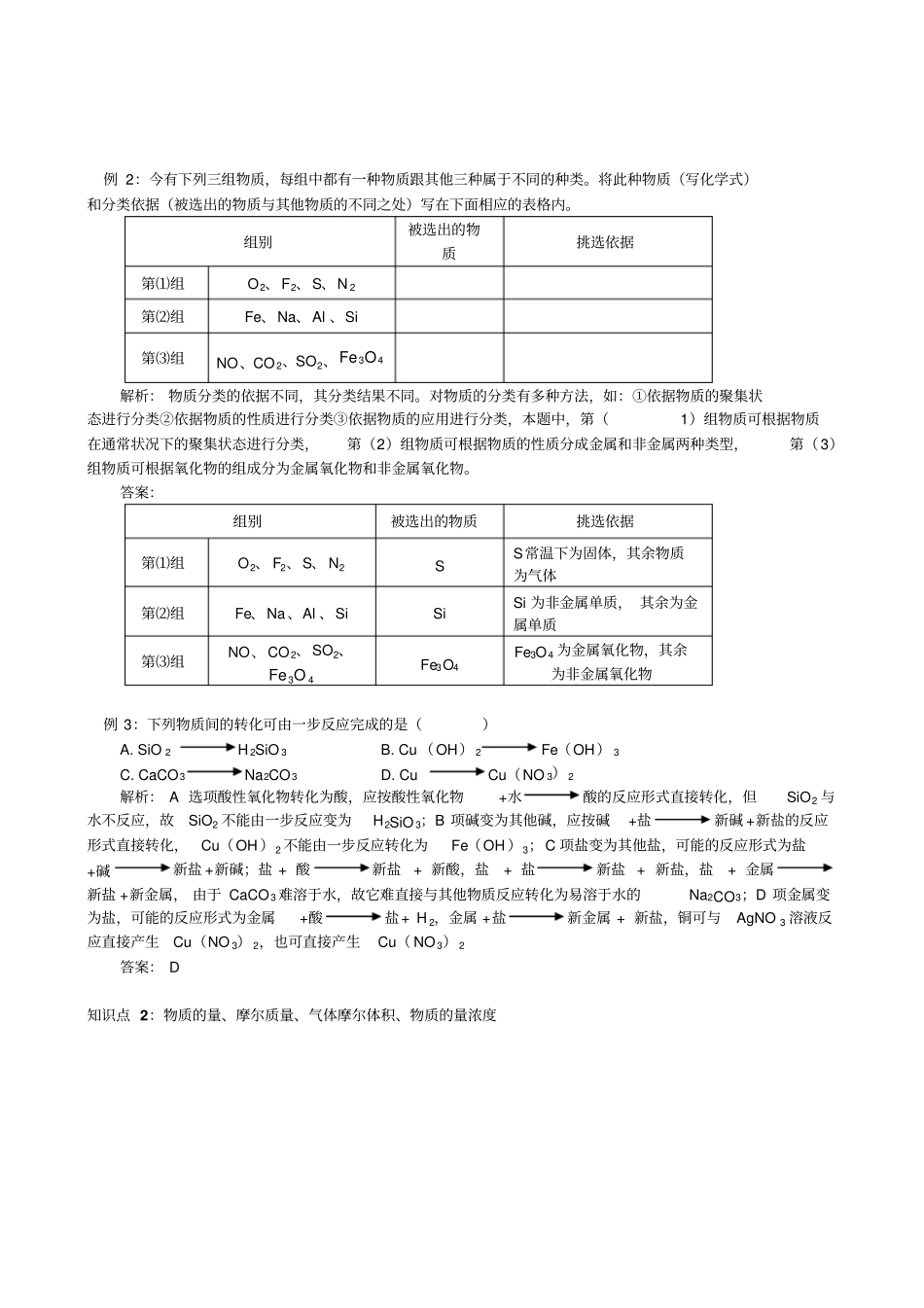
无机物之间的转化〔七类物质反应的相互关系表,便于书写化学方程式〕说明:①酸:根据是否含有氧元素分为含氧酸,如:H2SO4 和无氧酸,如HCl ;也可根据电离程度分为强酸,如 HCl 、H 2SO4、HNO 3 和弱酸,如H2SO3、H2CO3、HClO ;又可根据电离出的氢离子数目分为:一元酸,如 HCl 、HNO 3;二元酸,如H2SO4、H 2CO 3 和三元酸,如H3PO4 等
还可根据是否有挥发性分为挥发性酸HCl 、HNO 3 和难挥发性酸H2SO4 等,或根据成酸元素是否具有氧化性,分为氧化性酸,如HNO 3、H 2SO4和非氧化性酸,如HCl 、H2CO 3 等②酸性氧化物不一定都是非金属氧化物,如高价态的金属氧化物:Mn 2O7;非金属氧化物也不一定是酸性氧化物,如CO、NO 等③碱性氧化物都是金属氧化物,但金属氧