第 9 讲水溶液中的离子平衡[限时 50 分钟,满分 70 分]一、选择题(包括 7 个小题,每小题 5 分,共 35 分)1.(2016·上海高考)能证明乙酸是弱酸的实验事实是A.CH3COOH 溶液与 Zn 反应放出 H2B.0
1 mol·L CH3COONa 溶液的 pH 大于 7C.CH3COOH 溶液与 Na2CO3反应生成 CO2D.0
1 mol·L CH3COOH 溶液可使紫色石蕊变红解析A.只能证明乙酸具有酸性,不能证明其酸性强弱,错误;B
该盐水溶液显碱性,由于 NaOH 是强碱,故可以证明乙酸是弱酸,正确;C
可以证明乙酸的酸性比碳酸强,但是不能证明其酸性强弱,错误;D
可以证明乙酸具有酸性,但是不能证明其酸性强弱,错误
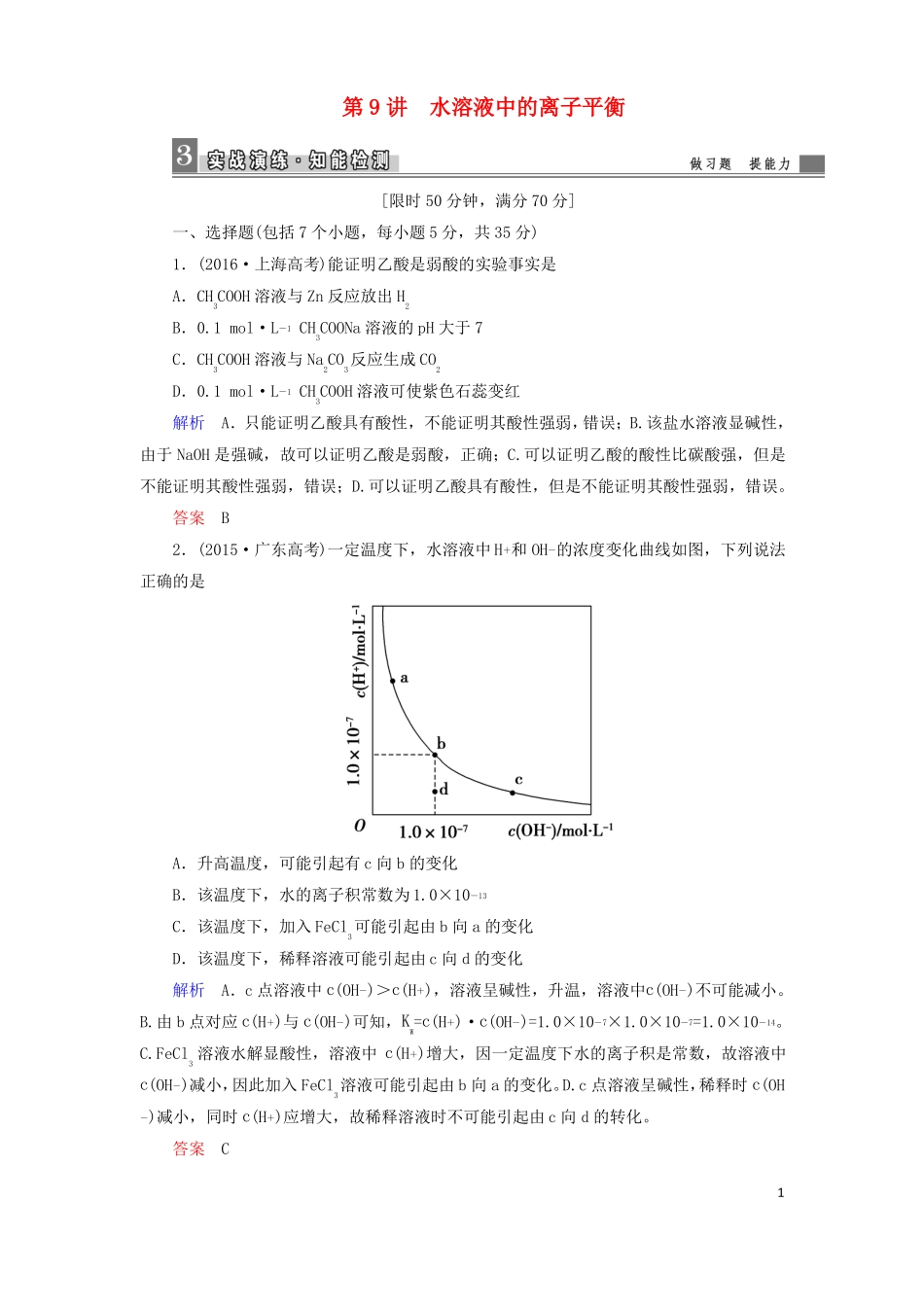
答案B2.(2015·广东高考)一定温度下,水溶液中 H 和 OH 的浓度变化曲线如图,下列说法正确的是+--1-1A.升高温度,可能引起有 c 向 b 的变化B.该温度下,水的离子积常数为 1
0×10-13C.该温度下,加入 FeCl3可能引起由 b 向 a 的变化D.该温度下,稀释溶液可能引起由 c 向 d 的变化解析A.c 点溶液中 c(OH )>c(H ),溶液呈碱性,升温,溶液中c(OH )不可能减小
由 b 点对应 c(H )与 c(OH )可知,KW=c(H )·c(OH )=1
0×10 ×1
0×10 =1
0×10++-+--7-7-14-+-
FeCl3 溶液水解显酸性,溶液中 c(H )增大,因一定温度下水的离子积是常数,故溶液中c(OH-)减小,因此加入 FeCl3溶液可能引起由 b 向 a 的变化
c 点溶液呈碱性,稀释时 c(OH-)减小,同时 c(H )应增大,故稀释溶液时不可能引起由 c 向 d 的转化
答案C1+3.(2015·山东高考)室温下向 10 mL 0
1 mol·L Na