水中钙镁离子含量测定实验十四水硬度的测定一实验目的1、了解硬度的常用表示方法;2、学会用配位滴定法测定水中钙镁含量,钙含量的原理和方法3、掌握铬黑 T,钙指示剂的使用条件和终点变化
二、实验原理1、总硬度、钙硬度、镁硬度的概念及表示方法;水的硬度主要是指水中含可溶性的钙盐和镁盐
总硬度通常以每 L 水中含的碳酸钙的 mg 数,即 mg/L
钙硬度即每 1L 水中含的钙离子的 mg 数,mg/L
镁硬度即每 1L 水中含的镁离子的 mg 数,mg/L2总硬度的测定条件与原理测定条件:以 NH-NHC1 缓冲溶液控制溶液 pH=10,以铬黑 T 为指示剂,用 EDTA34滴定水样
原理:滴定前水样中的钙离子和镁离子与加入的铬黑 T 指示剂络合,溶液呈现酒红色,随着 EDTA 的滴入,配合物中的金属离子逐渐被 EDTA 夺出,释放出指示剂,使溶液颜色逐渐变蓝,至纯蓝色为终点,由滴定所用的 EDTA 的体积即可换算出水样的总硬度
3钙硬度的测定条件与原理;测定条件:用 NaOH 溶液调节待测水样的 pH 为 13,并加入钙指示剂,然后用 EDTA滴定
原理:调节溶液呈强碱性以掩蔽镁离子,使镁离子生成氢氧化物沉淀,然后加入指示剂用 EDTA 滴定其中的钙离子,至酒红色变为纯蓝色即为终点,由滴定所用的 EDTA 的体积即可算出水样中钙离子的含量,从而求出钙硬度
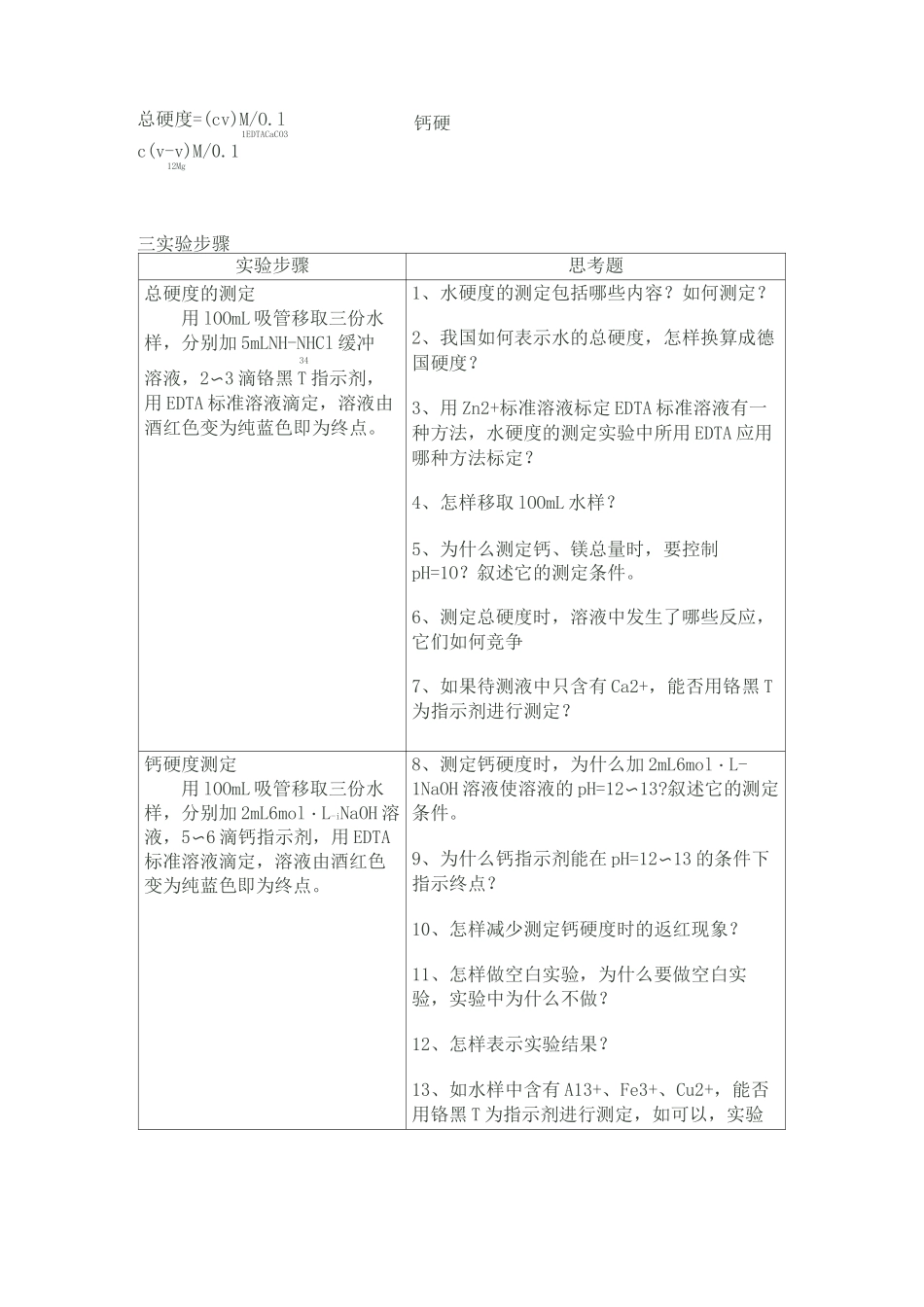
4、相关的计算公式钙硬总硬度=(cv)M/O
l1EDTACaCO3c(v-v)M/0
112Mg三实验步骤实验步骤思考题总硬度的测定用 lOOmL 吸管移取三份水样,分别加 5mLNH-NHCl 缓冲34溶液,2〜3 滴铬黑 T 指示剂,用 EDTA 标准溶液滴定,溶液由酒红色变为纯蓝色即为终点
1、水硬度的测定包括哪些内容
2、我国如何表示水的总硬度,怎样换算成德国硬度
3、用 Zn2+标准溶液标定 EDTA 标准