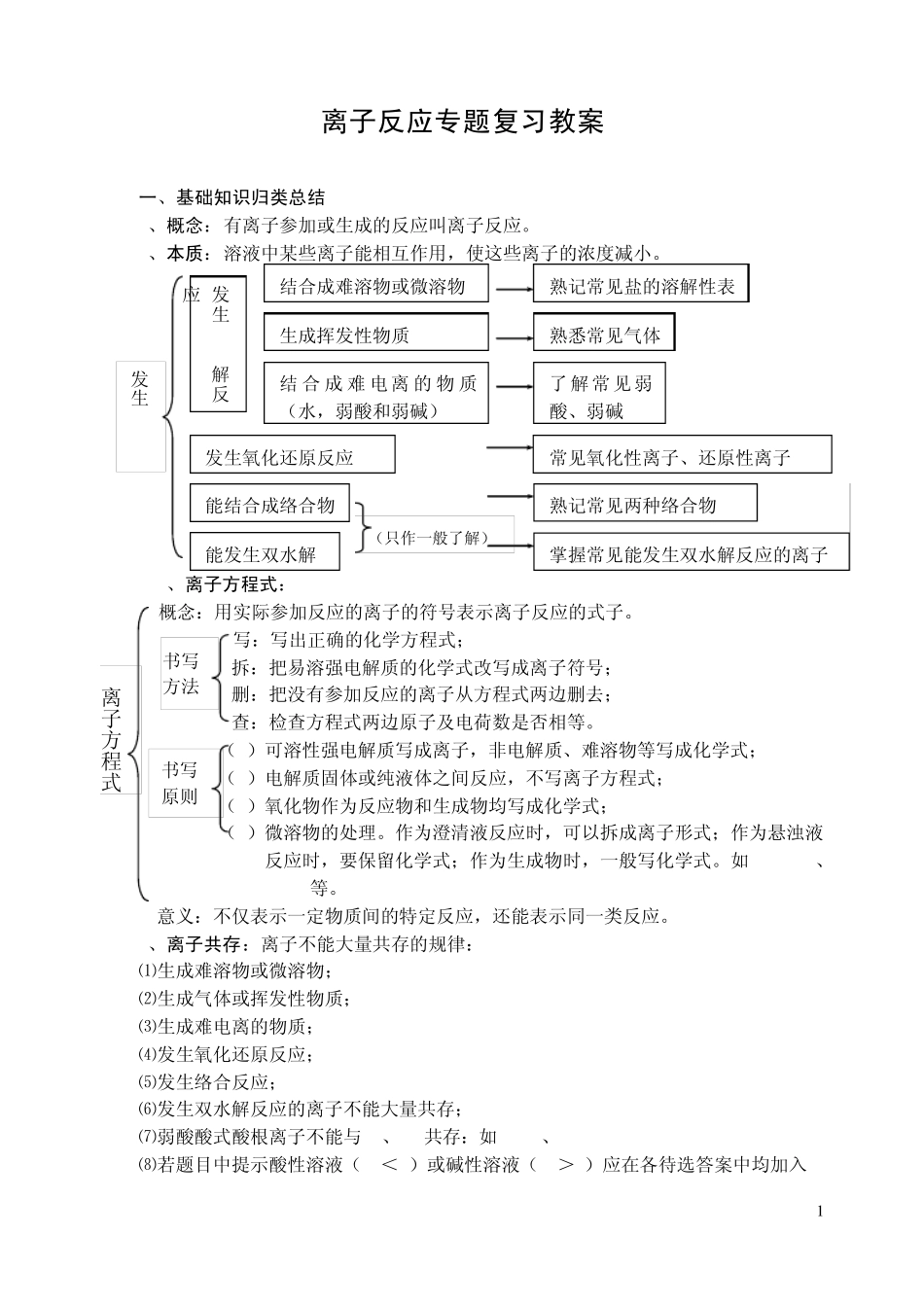
1 离子反应专题复习教案 一、基础知识归类总结 1、概念:有离子参加或生成的反应叫离子反应
2、本质:溶液中某些离子能相互作用,使这些离子的浓度减小
3、离子方程式: 概念:用实际参加反应的离子的符号表示离子反应的式子
写:写出正确的化学方程式; 拆:把易溶强电解质的化学式改写成离子符号; 删:把没有参加反应的离子从方程式两边删去; 查:检查方程式两边原子及电荷数是否相等
(1)可溶性强电解质写成离子,非电解质、难溶物等写成化学式; (2)电解质固体或纯液体之间反应,不写离子方程式; (3)氧化物作为反应物和生成物均写成化学式; (4)微溶物的处理
作为澄清液反应时,可以拆成离子形式;作为悬浊液反应时,要保留化学式;作为生成物时,一般写化学式
如Ca(OH)2、CaSO4等
意义:不仅表示一定物质间的特定反应,还能表示同一类反应
4、离子共存:离子不能大量共存的规律: ⑴生成难溶物或微溶物; ⑵生成气体或挥发性物质; ⑶生成难电离的物质; ⑷发生氧化还原反应; ⑸发生络合反应; ⑹发生双水解反应的离子不能大量共存; ⑺弱酸酸式酸根离子不能与 H+、OH-共存:如HCO3-、HS- ⑻若题目中提示酸性溶液(pH<7)或碱性溶液(pH>7)应在各待选答案中均加入 H+书写 原则 离子方程式 书写 方法 发生条件 结合成难溶物或微溶物 生成挥发性物质 结 合 成难电离的物质(水,弱酸和弱碱) 发生氧化还原反应 能结合成络合物 能发生双水解 熟记常见盐的溶解性表 熟悉常见气体 了解常见弱酸、弱碱 常见氧化性离子、还原性离子 熟记常见两种络合物 掌握常见能发生双水解反应的离子 发生复分解反应(只作一般了解) 2 或OH-后考虑
⑼溶液无色透明时,则溶液中肯定没有有色离子
常见的有色离子是Cu2+、Fe3+、Fe2+、MnO4-等
5、思维拓展 例1、下列离子方程式中,