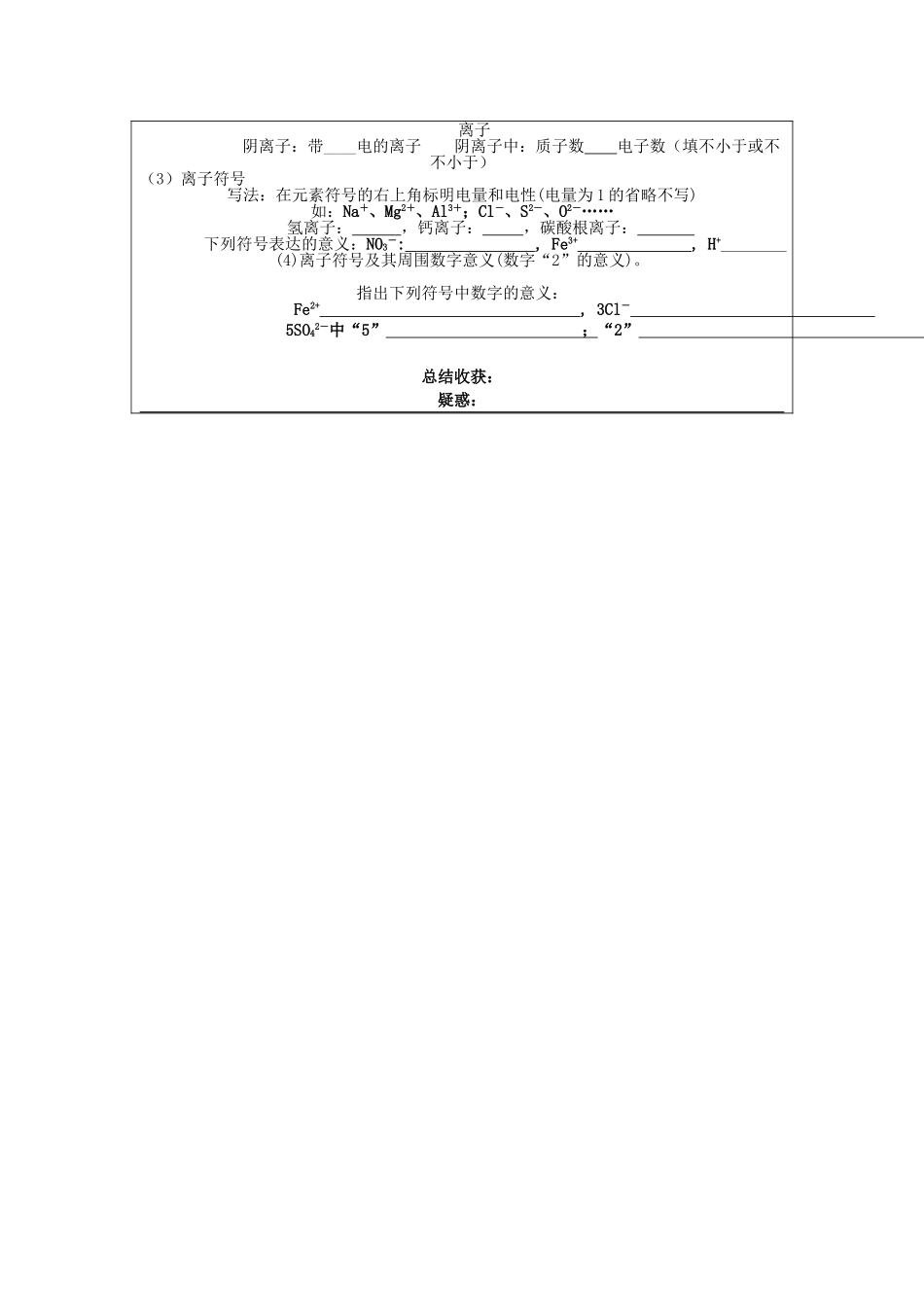
离子目的:1、初步理解原子核外的电子是分层排布的和原子构造的表达措施。2、理解原子构造与元素化学性质的关系以及核外电子的排布规律3、初步体会物质构成的奥秘,,培养学生的空间想象能力,抽象思维能力和分析推理能力。树立“构造决定性质”,“物质的微粒性”等辩证唯物主义观点。重点:1.原子构造与元素化学性质的关系,2.核外电子排布的概念难点:同重点学法指导: 认真阅读教材,结合导学案深入理解,重视挖掘图表的含义。知识链接:1、跟___、___同样,离子也是构成物质的一种粒子。2、在原子中,质子数=____________=___________=_____________3、元素的种类是由_______________决定的。导学过程:朗诵《漫游原子世界》,猜想原子核外电子是怎样运动的呢?它们能否挣脱原子核的吸引呢?“我是一种小、小、小的电子,在原子内部很大的空间中围绕着原子核这个小老头不停地转动;我们在飞,却怎么也飞不高。由于这老头长得很尤其:虽然占据原子中央很小的地盘,却是由中子和质子构成,中子不带电,质子带正电,因此,这小老头也带正电,很有能耐,恰好把我们身上的负电深深吸引,因此我们很难脱离原子核的怀抱。”自主探究:知识点一:核外电子的排布【阅读】书本 P78~79图文,思考下列问题:1.核外电子是 排布的。2.画出钠原子的原子构造示意图,并阐明各部分表达的含义:①圆圈表达 、②圆圈内+表达 、③数字表达 、④弧线表达 、⑤弧线上的数字表达 。(原子构造示意图中有五个要素)3.请分别画出质子数为 2, 6,9, 13,16, 18 的元素原子构造示意图。4.仔细研究 1—18 号元素原子构造示意图(下图),我们发现原子核外电子的排布特点是:第一层最多排 个电子,第二层最多排 个电子,第一层 后排第二层,第二层 后排第三层;最外层最多排 个电子。5. 相对稳定构造:最外层具有 电子(只有一种电子层的元素具有 2 个电子)的构造属于相对稳定构造。6.深入的探究发现:元素的最外层电子数与元素的性质的关系元素分类最外层电子数得失电子倾向化学性质稀有气体元素8 个(He 为 2 个)不易得失、相对稳定稳定金属元素一般 4 个 易 最外层电子不稳定非金属元素一般 个 易 电子不稳定★对照原子构造示意图,思考:O 与 S、F 与 Cl 两组元素的化学性质怎样?__________________________________________________________________■元素的化学性质与原子的 数关系亲密;最外层电子数相等的元素,它...