国家食品药品监督管理局公 告2024 年 第 65 号关于发布药物临床试验机构资格认定复核检查标准的公告 为切实做好药物临床试验机构资格认定复核工作,落实讨论机构监督检查和品种核查相结合的工作要求,根据我局和卫生部《关于开展药物临床试验机构资格认定复核检查工作的通知》(国食药监注〔2024〕203 号)要求,我局组织有关部门和相关专家制定了《药物临床试验机构资格认定复核检查标准》,现予以发布,自发布之日起施行
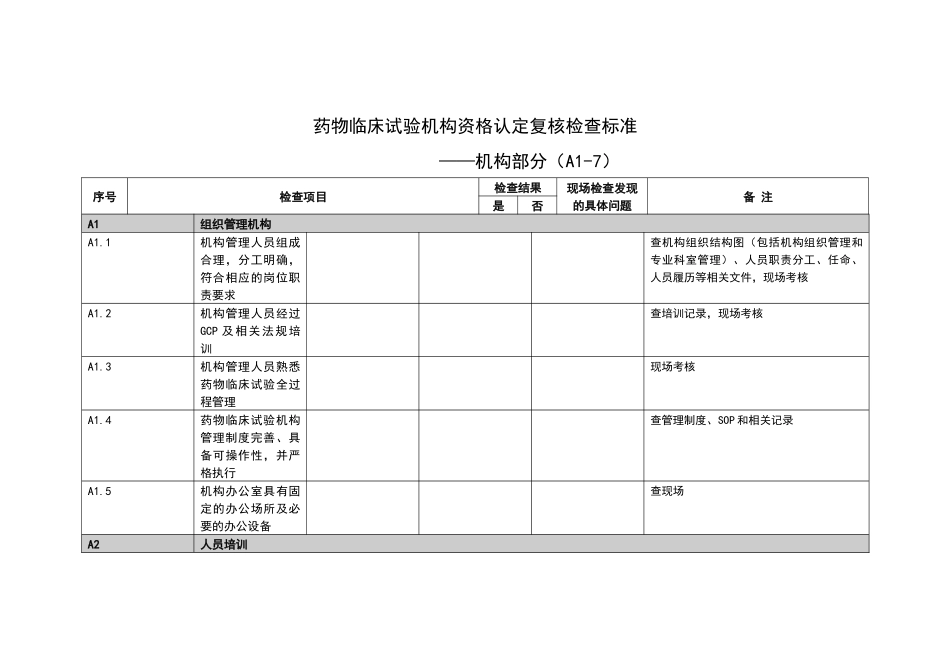
国家食品药品监督管理局 二○○九年十一月二日药物临床试验机构资格认定复核检查标准 ——机构部分(A1-7)序号检查项目检查结果现场检查发现的具体问题备 注是否A1组织管理机构A1
1机构管理人员组成合理,分工明确,符合相应的岗位职责要求查机构组织结构图(包括机构组织管理和专业科室管理)、人员职责分工、任命、人员履历等相关文件,现场考核A1
2机构管理人员经过GCP 及相关法规培训查培训记录,现场考核A1
3机构管理人员熟悉药物临床试验全过程管理现场考核A1
4药物临床试验机构管理制度完善、具备可操作性,并严格执行查管理制度、SOP 和相关记录A1
5机构办公室具有固定的办公场所及必要的办公设备查现场A2人员培训序号检查项目检查结果现场检查发现的具体问题备 注是否A2
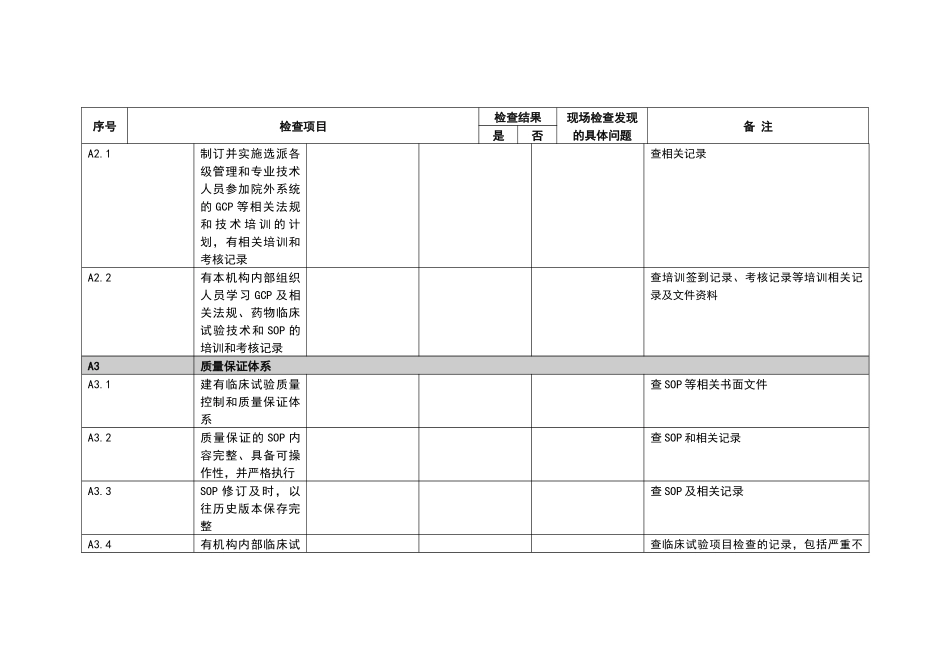
1制订并实施选派各级管理和专业技术人员参加院外系统的 GCP 等相关法规和 技 术 培 训 的 计划,有相关培训和考核记录查相关记录A2
2有本机构内部组织人员学习 GCP 及相关法规、药物临床试验技术和 SOP 的培训和考核记录查培训签到记录、考核记录等培训相关记录及文件资料A3质量保证体系A3
1建有临床试验质量控制和质量保证体系查 SOP 等相关书面文件A3
2质量保证的 SOP 内容完整、具备可操作性,并严格执行查 SOP 和相关记录A3
3SOP 修订及时,以往历史版本保存完整查