2013 年高考化学一轮复习教学教案:1
2《原子结构与元素的性质》第 2 课时(人教版选修 3)学习目标:1
知道原子结构模型的发展; 2
进一步认识原子核外电子的分层排布;3
知道原子核外电子的能层分布及其能量关系;4
知道原子核外电子的能级分布及其能量关系;5
能用符号表示原子核外的不同能 级,初步知道量子数的涵义;6
识记常见元素(1~36 号);7
知道原子结构的构造原理,能用构造原理认识原子的核外电子排布
导学提纲:1
(自学、思考)元素周期表中同周期主族元素从左到右,原子半径的变化趋势如何
应如何理解这种趋势
元素周期表中,同主族元素从上到下,原子半径 的变化趋势如何
应如何理解这种趋势
(自学、思考)什么是第一电离能
如何理解第二电离能 I2、第三电离能 I3 、I4、I5……
气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量叫做第一电离能(用 I1表示),从一价气态基态正离子中再失去一个电子所需消耗的能量叫做第二电离能(用 I2表示),依次类推,可得到 I3、I4、I5……同一种元素的逐级电离能的大小关系:I1<I2<I3<I4<I5……即一个原子的逐级 电离能是逐渐增大的
这是因为随着电子的逐个失去,阳离子所带的正 电荷数越来越大,再要失去一个电子需克服的电性引力也越来越大,消耗的能量也越来越多
(思考、讨论)原子的第一电离能有什么变化规律呢
碱金属元素的第一电离能有什么变化规律呢
为什么 Be 的第一电离能大于 B,N 的第一电离能大于 O,Mg 的第一电离能大于 Al,Zn 的第一电离能大于 Ga
第一电离能的大小与元素的金属性和非金属性有什么关系
碱金属的电离能与金属活泼性有什么关系
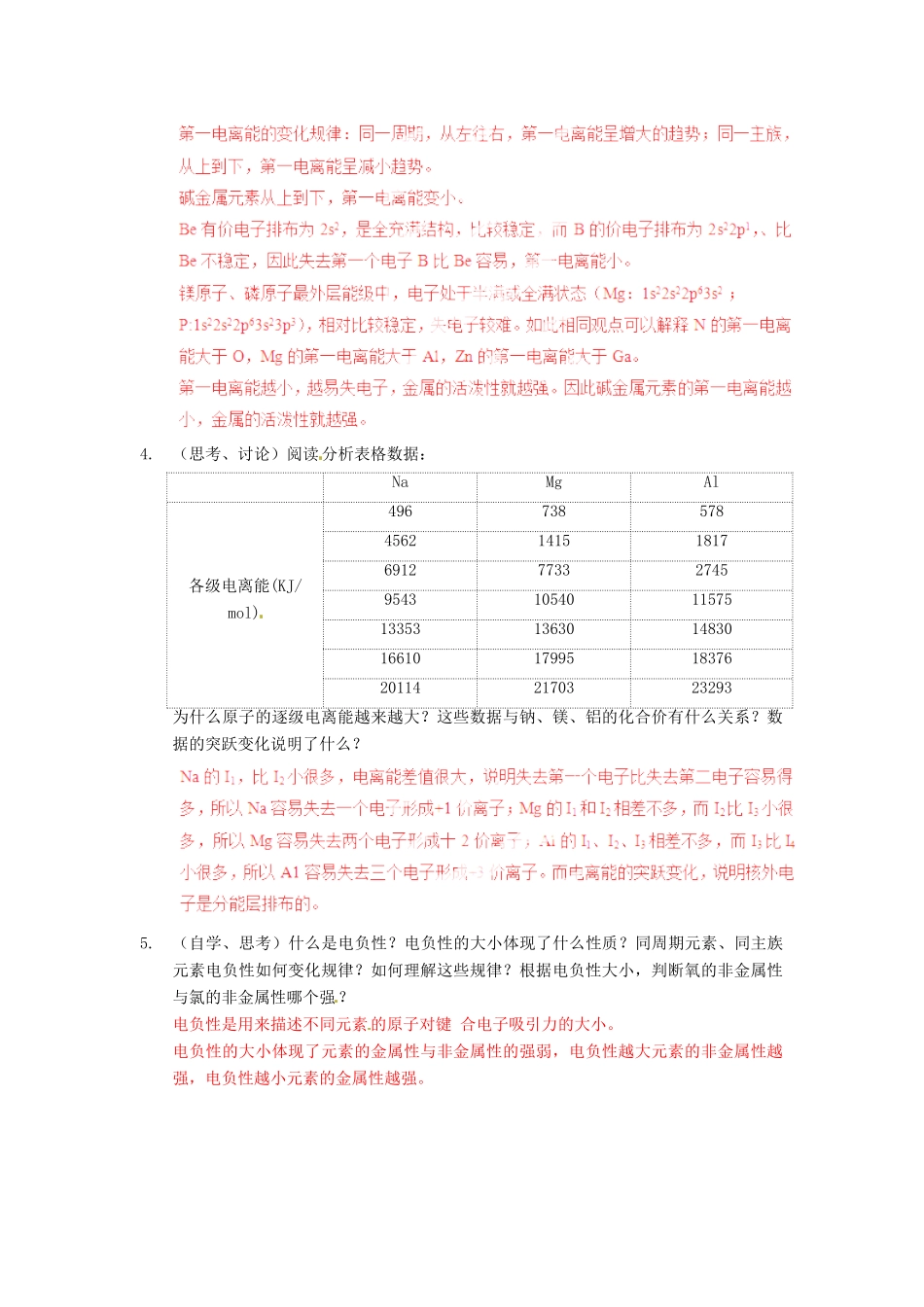
(思考、讨论)阅读分析表格数据:NaMgAl各级电离能(KJ/mol)49673857845621415181769127733274