题型一基本概念、基本理论的综合应用1
(2018·韶关市高三4月模拟考试)NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划
(1)催化剂常具有较强的选择性
已知:反应Ⅰ:4NH3(g)+5O2(g)4NO(g)+6H2O(g)ΔH1=-905kJ·mol-1反应Ⅱ:4NH3(g)+3O2(g)2N2(g)+6H2O(g)ΔH2=-1266
6kJ·mol-1写出NO分解生成N2与O2的热化学方程式:__________________________________________________________________________________________________________
(2)N2O也可分解生成N2与O2
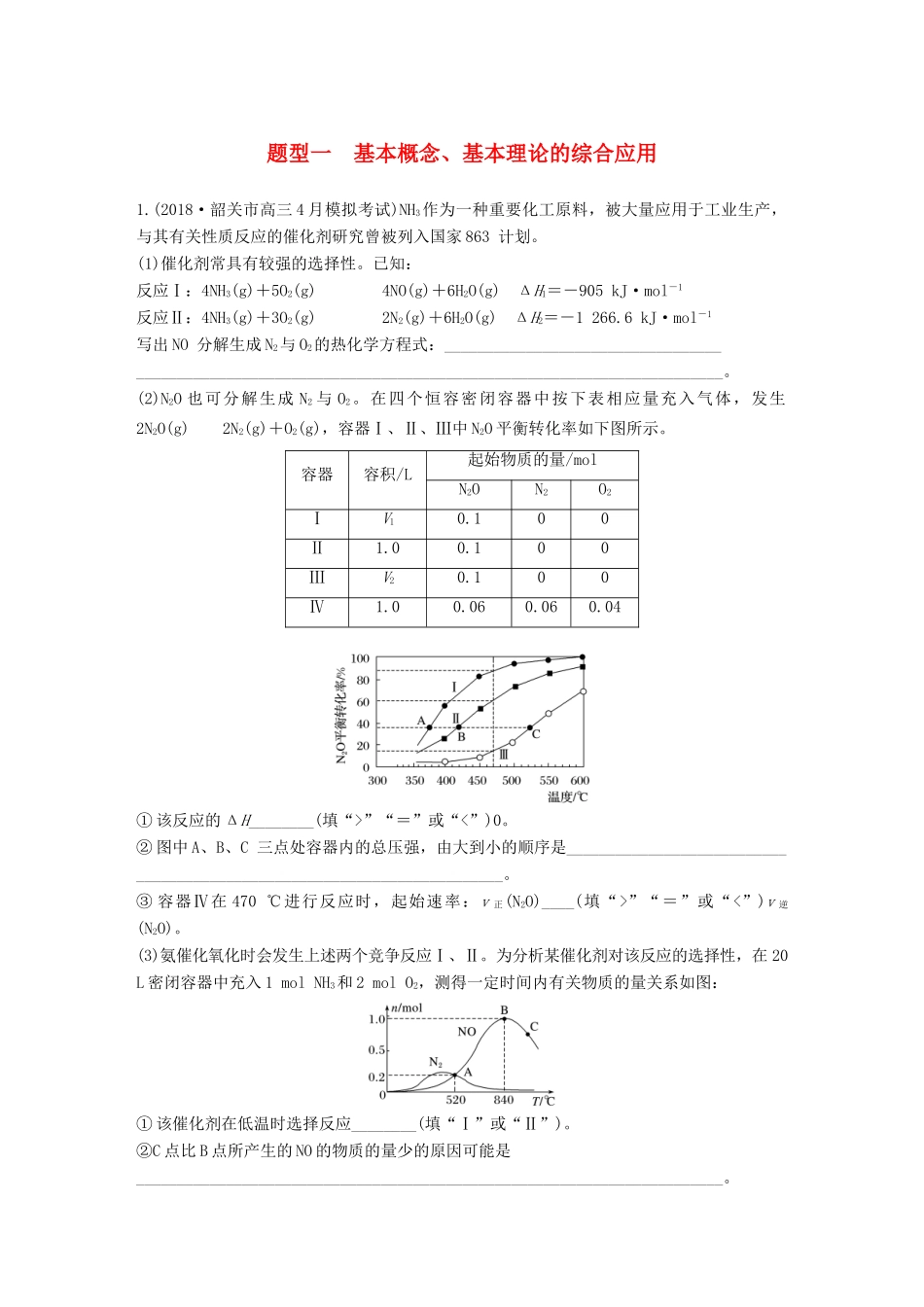
在四个恒容密闭容器中按下表相应量充入气体,发生2N2O(g)2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O平衡转化率如下图所示
容器容积/L起始物质的量/molN2ON2O2ⅠV10
100ⅢV20
04①该反应的ΔH________(填“>”“=”或“”“=”或“②p(C)>p(B)>p(A)(或C>B>A)③>(3)①Ⅱ②该反应为放热反应,温度升高,平衡向逆反应方向移动或催化剂活性降低解析(1)NO分解生成N2与O2的方程式为2NO(g)N2(g)+O2(g),根据已知的反应Ⅰ和反应Ⅱ,要得到该方程,则,即ΔH==kJ·mol-1=-180
8kJ·mol-1
(2)①根据图像,温度升高,转化率增大,则平衡向右移动,说明正反应方向吸热,则反应的ΔH>0
②A、B、C三点中N2O的转化率相同,则容器中反应物、生成物的量均相同,则容器的压强取决于容器的体积,根据图像,相同温度时:转化率大小为:Ⅰ>Ⅱ>Ⅲ,则