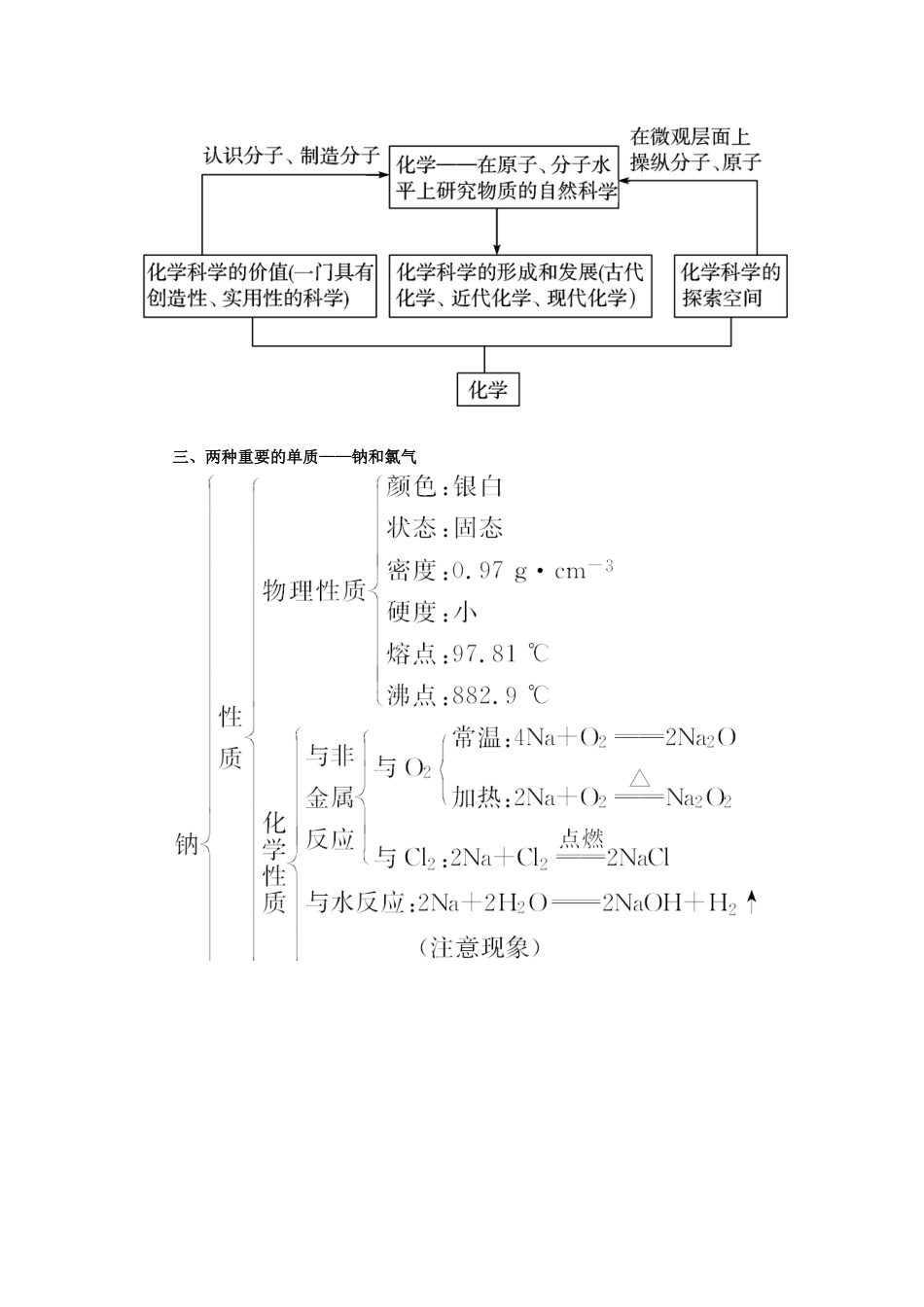
【金版学案】2014-2015 学年高中化学 第一章 章末知识整合 鲁科版必修 1一、本章教材内容框架认识化学科学 二、化学科学的概念、特征及发展三、两种重要的单质——钠和氯气四、以物质的量为中心的物理量之间的联系专题一 有关 Na2O2跟 CO2、H2O 反应的计算技巧1
在这两个反应中,对 Na2O2固体而言,反应①中 Na2O2固体增重的质量实际上是 H2O 中 H的质量,其结果可看做是 H2O 中的 H 进入到了 NaOH 中,而 O 转化成了 O2逸出
同样道理,在反应②中,Na2O2增重的质量实际上是 2CO 的质量,因为 2CO2可写成 2 个CO 和 1 个 O2的形式
2.若某物质 W g,完全燃烧,通过足量的 Na2O2固体,反应完毕,固体质量增重为 W g,则该物质的通式为(CO)mHn(m=0,1,2,3,…;n=1,2,3,…)
原因:①+②得:2CO+2Na2O2===2Na2CO3;③+④得:2H2+2Na2O2===4NaOH
根据反应原理,概括为把 CO 或 H2“吃”进去,故质量增加的量就是原物质的质量
因此只要该物质中 C 和 O 的物质的量之比为 1∶1 即可
如常见物质有:CO、H2、CH3COOH(醋酸)等
专题二 平均相对分子质量的求法1.已知标准状况时气体密度 ρ,M=22
2.已知非标准状况气体温度、压强、密度,M=
3.已知两种气体的相对密度 D,MA = DMB;气体的相对密度:D==
4.混合气体的平均式量(n1,n2,…表示混合物中各组分的物质的量;V1,V2,…表示混合物中各组分的体积;M1,M2,…表示混合物中各组分的式量):混合气体本来无式量,但对组成一定的混合气体来说,可以根据其各组的组成和 式量来计算所谓的平均式量
它在数值上等于混合气体的平均摩尔质量,其表达式为:===M1·n1%+M2·n2%+