第一节 钠及其化合物考纲定位核心素养1
了解钠的主要性质及其应用
掌握钠的重要化合物(Na2O2、NaOH、Na2CO3、NaHCO3等)的主要性质及其应用
了解钠及其重要化合物的制备方法
了解 Na+、K+的检验方法
宏观辨识——认识钠及其化合物的性质和应用
微观探析——能从钠的原子结构理解其性质,领悟结构决定性质
科学探究——领悟钠及其化合物的性质探究方案,并实验探究过程
模型认知——以钠及其化合物的反应,利用“差量法”进行有关计算,利用图像法进行分析
考点一| 钠及其氧化物1.钠的主要性质及应用(1)物理性质:银白色,金属光泽,ρ=0
97 g/cm3,比水的密度小、比煤油的密度大,质软,熔点为 97
81 ℃,沸点为 882
(2)化学性质(写出化学方程式)① 与非金属反应② 与 H2O 反应:2Na + 2H 2O == = 2NaOH + H 2↑
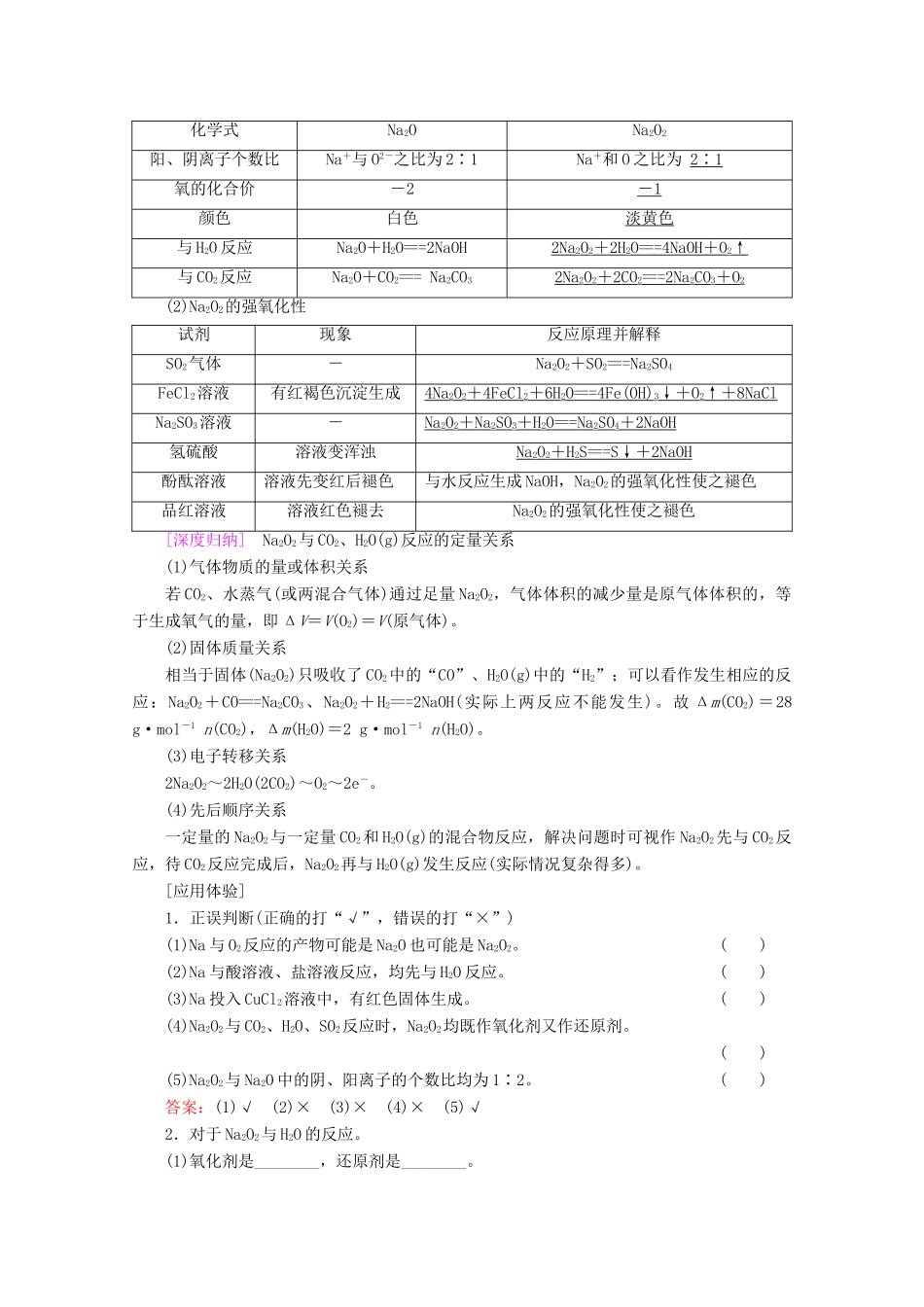
实验探究:Na 与 H2O(含酚酞)反应的现象及解释③ 与乙醇反应:2Na+2C2H5OH―→2C2H5ONa+H2↑
④ 与酸(HCl)反应:2Na + 2HCl == = 2NaCl + H 2↑
⑤ 与盐(CuSO4)溶液反应:2Na + 2H 2O == = 2NaOH + H 2↑,CuSO4+ 2NaOH == = Cu(OH) 2↓ + Na2SO4(答案合理即可)
⑥ 与熔融盐 TiCl4反应:4Na+TiCl4=====Ti+4NaCl
(3)钠的保存与用途① 保存:少量钠保存在煤油或石蜡油中
② 用途:2.钠的氧化物(1)氧化钠和过氧化钠化学式Na2ONa2O2阳、阴离子个数比Na+与 O2-之比为 2∶1Na+和 O 之比为 2∶1氧的化合价-2- 1 颜色白色淡黄色与 H2O 反应Na2O+H2O===2NaOH2Na2O2+ 2H 2O == = 4NaO