第九章 电化学基础[考纲解读] 1
理解原电池的构成、工作原理及应用
能书写出电极反应和总反应方程式
了解常见化学电源的种类及其工作原理
理解电解池的构成、工作原理及应用
了解金属发生电化学腐蚀的原因、金属腐蚀的危害以及防止金属腐蚀的措施
第 28 讲 原电池 化学电源一、原电池1.概念原电池是把□化学能转化为□电能的装置
2.构成条件(1)能自发进行的□氧化还原反应
(2)□活泼性不同的两电极
(3)形成闭合回路
形成闭合回路需三个条件:①□电解质溶液;②两电极直接或间接接触;③两电极插入□电解质溶液中
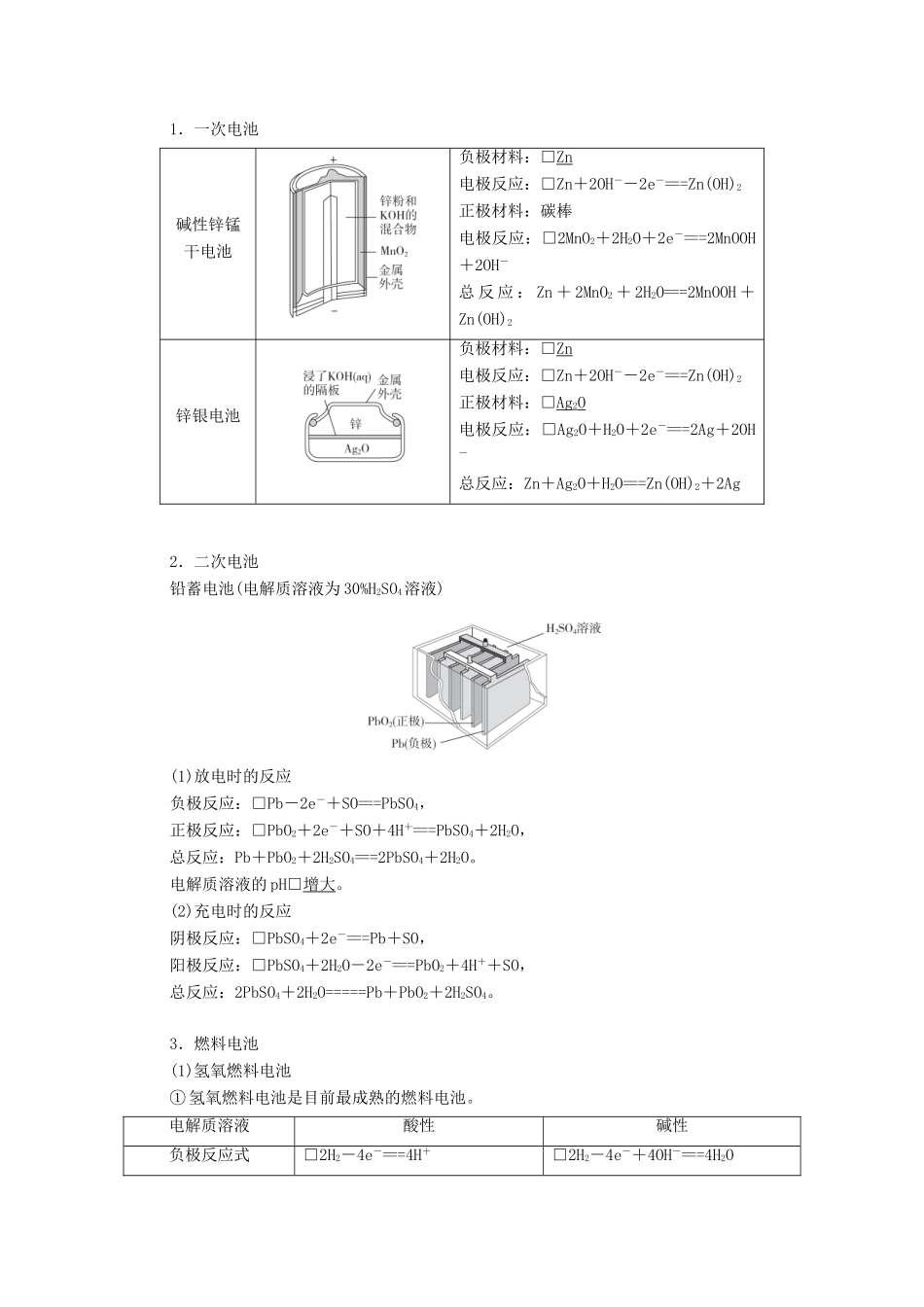
3.工作原理(以铜-锌原电池为例)装置图电极名称负极正极电极材料□锌片□铜片电极反应□Zn-2e-===Zn2+□Cu2++2e-===Cu反应类型□氧化反应□还原反应电子流向由□锌片沿导线流向□铜片电流方向由□铜片沿导线流向□锌片离子流向电解质溶液中,阴离子向□负极迁移,阳离子向□正极迁移盐桥中含有饱和 KCl 溶液,□K + 移向正极,□Cl - 移向负极电池反应方程式□Zn+Cu2+===Zn2++Cu两类装置的不同点还原剂 Zn 与氧化剂 Cu2+直接接触,既有化学能转化为电能,又有化学能转化为热能,造成能量损耗Zn 与氧化剂 Cu2+不直接接触,仅有化学能转化为电能,减少了能量损耗,故电流稳定,持续时间长二、化学电源1.一次电池碱性锌锰干电池负极材料:□Zn电极反应:□Zn+2OH--2e-===Zn(OH)2正极材料:碳棒电极反应:□2MnO2+2H2O+2e-===2MnOOH+2OH-总 反 应 : Zn + 2MnO2 + 2H2O===2MnOOH +Zn(OH)2锌银电池负极材料:□Zn电极反应:□Zn+2OH--2e-===Zn(OH)2正极材料:□Ag2O电极反应:□Ag2O+H2O+2e-===2Ag+2OH-总反应:Zn+Ag