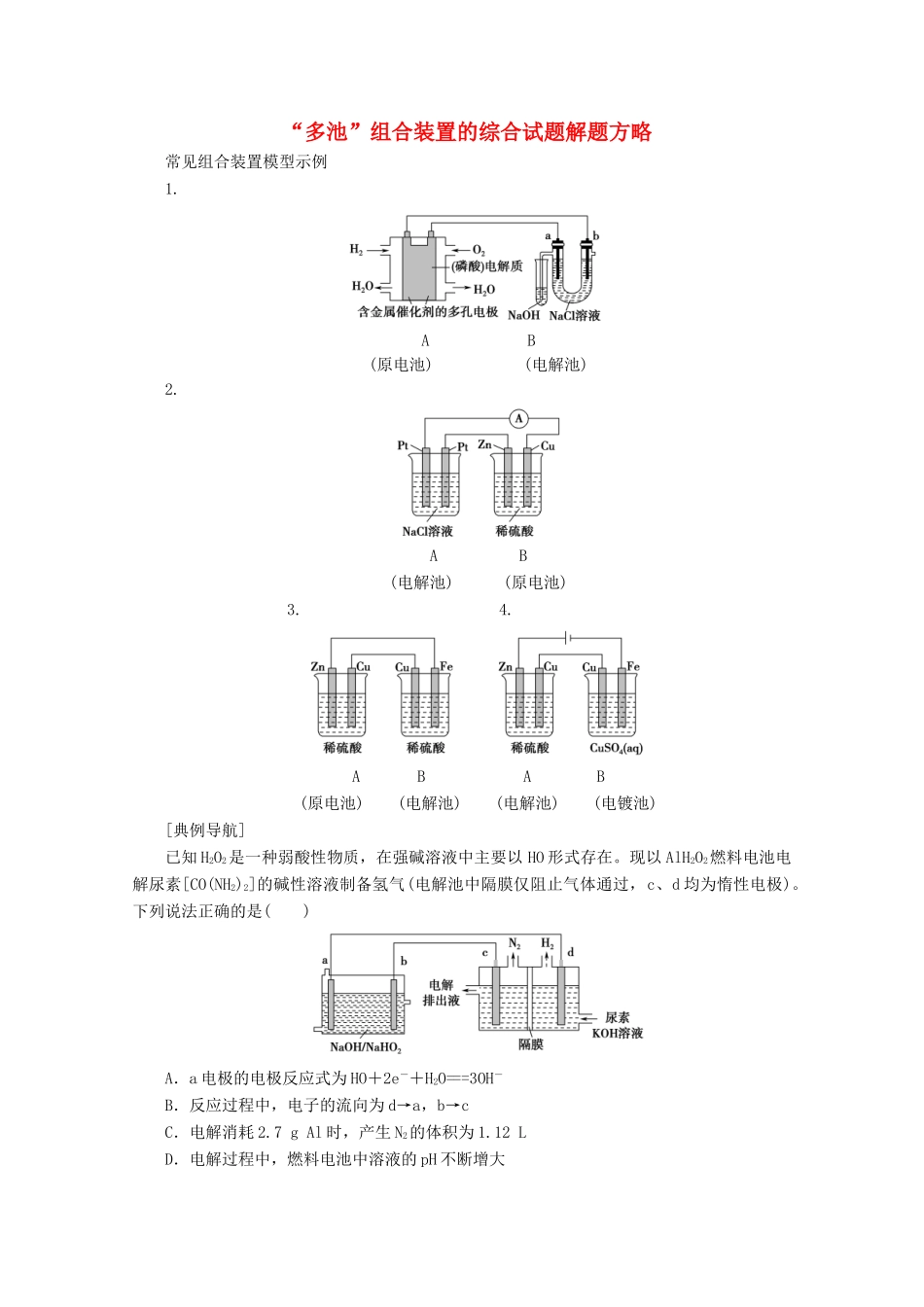
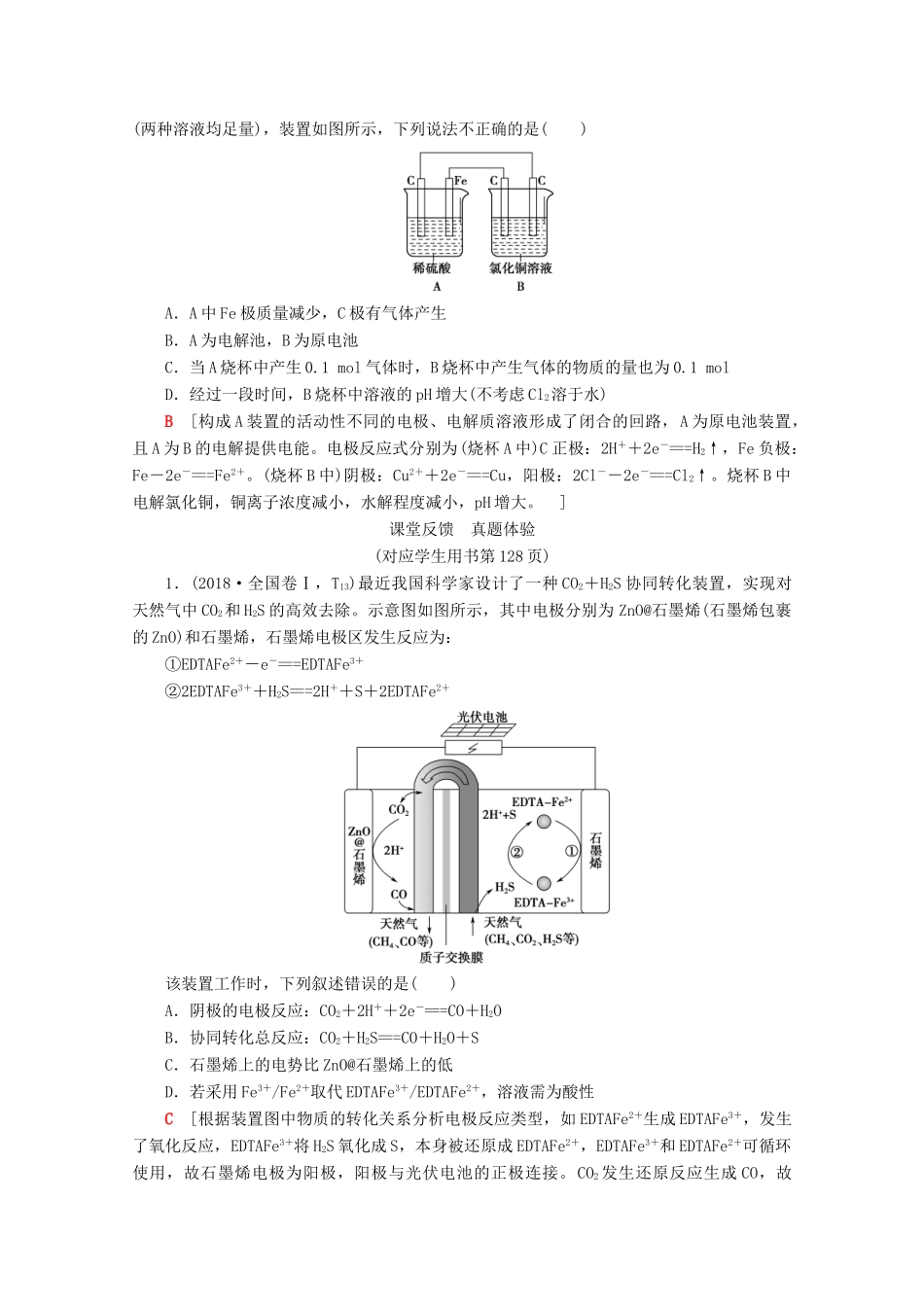
“多池”组合装置的综合试题解题方略常见组合装置模型示例1
A B(原电池) (电解池)2
A B(电解池) (原电池)3
A B A B(原电池) (电解池) (电解池) (电镀池)[典例导航]已知 H2O2是一种弱酸性物质,在强碱溶液中主要以 HO 形式存在
现以 AlH2O2燃料电池电解尿素[CO(NH2)2]的碱性溶液制备氢气(电解池中隔膜仅阻止气体通过,c、d 均为惰性电极)
下列说法正确的是( )A.a 电极的电极反应式为 HO+2e-+H2O===3OH-B.反应过程中,电子的流向为 d→a,b→cC.电解消耗 2
7 g Al 时,产生 N2的体积为 1
12 LD.电解过程中,燃料电池中溶液的 pH 不断增大[思路点拨] 左池为 AlH2O2燃料电池,右池为电解池→c 极为阳极[CO(NH2)2→N2],d 为阴极(H+→H2)→a 极为负极(Al→AlO),b 为正极(HO→OH-)
D [根据电解池中 c 极上发生氧化反应生成 N2知,c 极为阳极,故 d 极为阴极,所以 a极是负极,b 极为正极,a 极的电极反应式为 Al-3e-+4OH-===AlO+2H2O,A 错误;a 极为负极,b 极为正极,c 极为阳极,d 极为阴极,故反应过程中电子的流向为 a→d,c→b,B 错误;根据各电极上转移的电子数相等知,每消耗 0
1 mol Al,转移 0
3 mol 电子,生成 0
05 mol N2,在标准状况下 N2的体积为 1
12 L,但题中未标明标准状况,C 错误;AlH2O2燃料电池的总反应为 2Al+3HO===2AlO+OH-+H2O,反应中有 OH-生成,溶液 pH 增大,D 正确
]电极 a、b、c、d 的电极反应式分别为_________________________,_____________________________