第 12 讲 铜及其重要化合物、金属材料一、铜及其化合物1.铜的性质(1)物理性质:铜是紫红色金属,具有良好的导电性、导热性和延展性
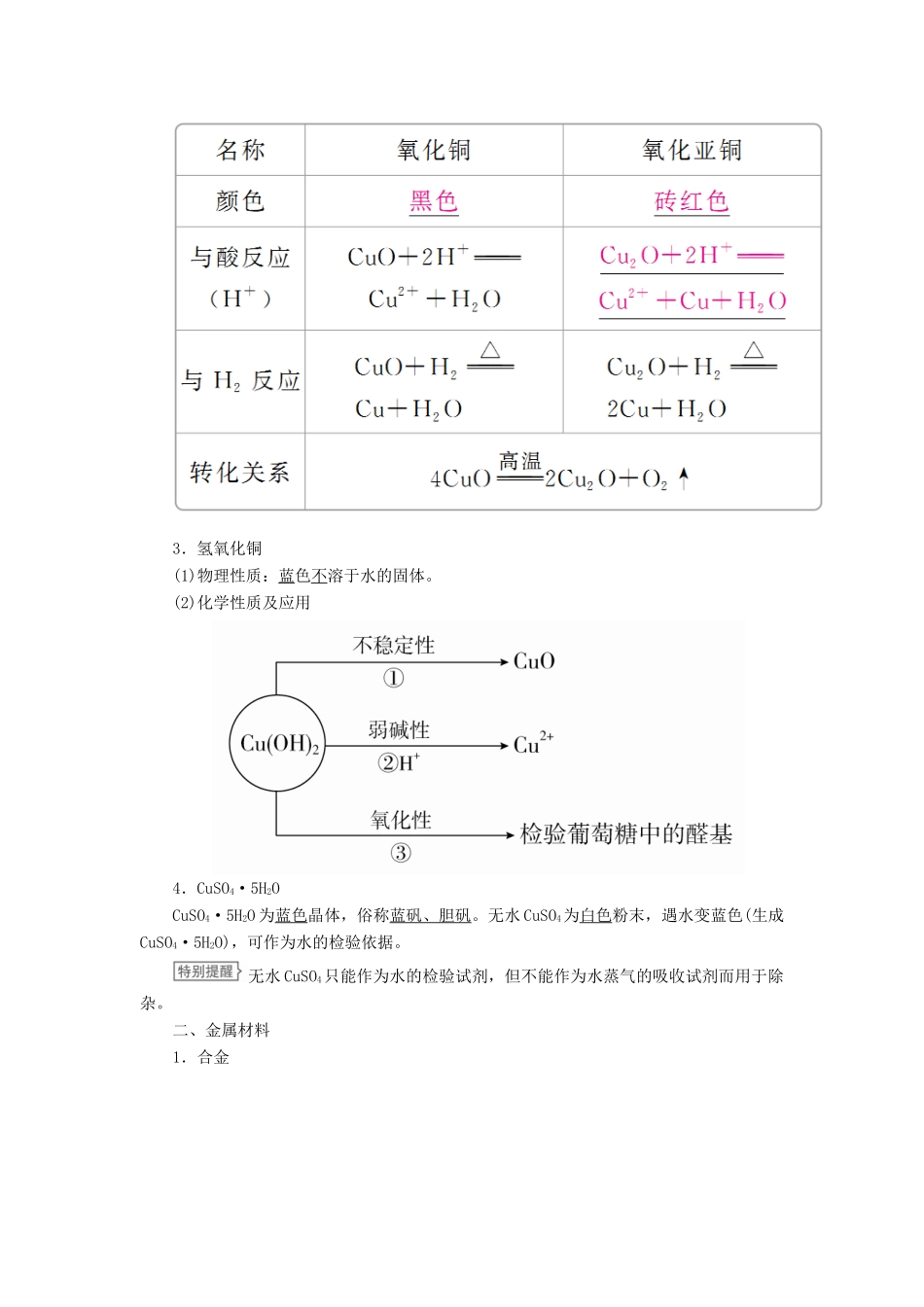
(2)化学性质写出图中有关反应的化学方程式或离子方程式:①2Cu+O2+CO2+H2O===Cu2(OH)2CO3②2Cu+S=====Cu2S2.氧化铜和氧化亚铜3.氢氧化铜(1)物理性质:蓝色不溶于水的固体
(2)化学性质及应用4.CuSO4·5H2OCuSO4·5H2O 为蓝色晶体,俗称蓝矾、胆矾
无水 CuSO4为白色粉末,遇水变蓝色(生成CuSO4·5H2O),可作为水的检验依据
无水 CuSO4只能作为水的检验试剂,但不能作为水蒸气的吸收试剂而用于除杂
二、金属材料1.合金2.常见金属材料(1)黑色金属材料——钢铁
① 钢是用量最大,用途最广的合金
(2)有色金属材料——铜和铝
① 我国使用最早的合金是青铜,常见的铜合金有黄铜和白铜
3.金属矿物的开发利用(1)金属在自然界中的存在(2)金属冶炼的一般步骤(3)金属冶炼的实质金属的冶炼过程就是把金属从化合态还原为游离态的过程
即 M n + + n e - = M
(4)金属冶炼的方法(用化学方程式表示)(5)铝热反应实验装置实验现象① 镁带剧烈燃烧,放出一定的热,并发出耀眼的白光,氧化铁和铝粉在较高温度下发生剧烈的反应;② 纸漏斗的下部被烧穿,有熔融物落入沙中实验结论高温下,铝与氧化铁发生反应,放出大量的热,反应的化学方程式为 2Al+Fe2O3=====2Fe+Al2O3原理应用① 制取熔点较高、活泼性弱于 Al 的金属铬、锰、钨等;② 金属焊接,如野外焊接钢轨等① 冶炼 Al 时只能电解 Al2O3不能电解 AlCl3(共价化合物,熔融时不导电)
加入冰晶石(Na3AlF6)的目的是降低 Al2O3的熔化温度
② 金属冶炼方法与金属活动性的关系:1.正误判断,正