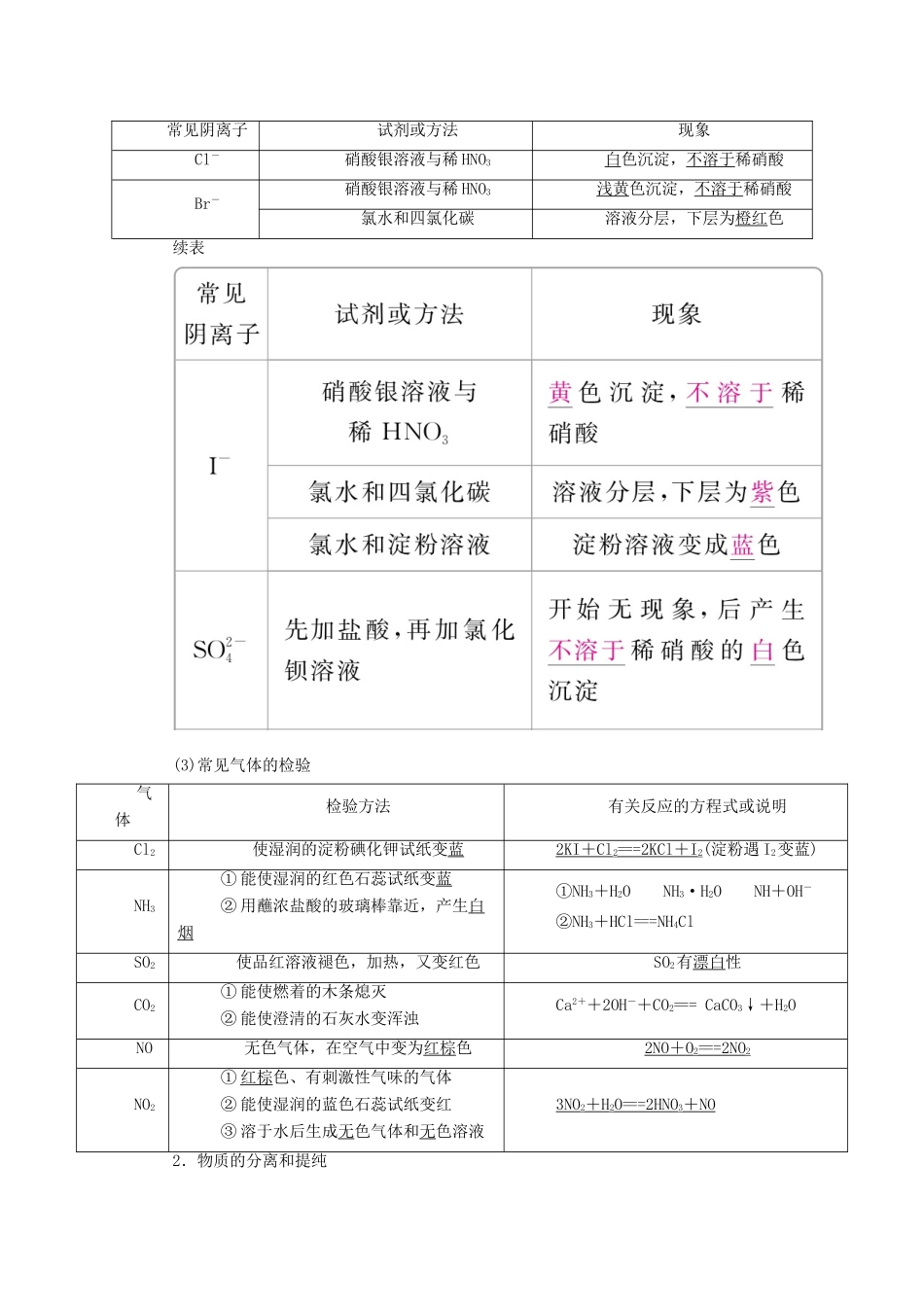
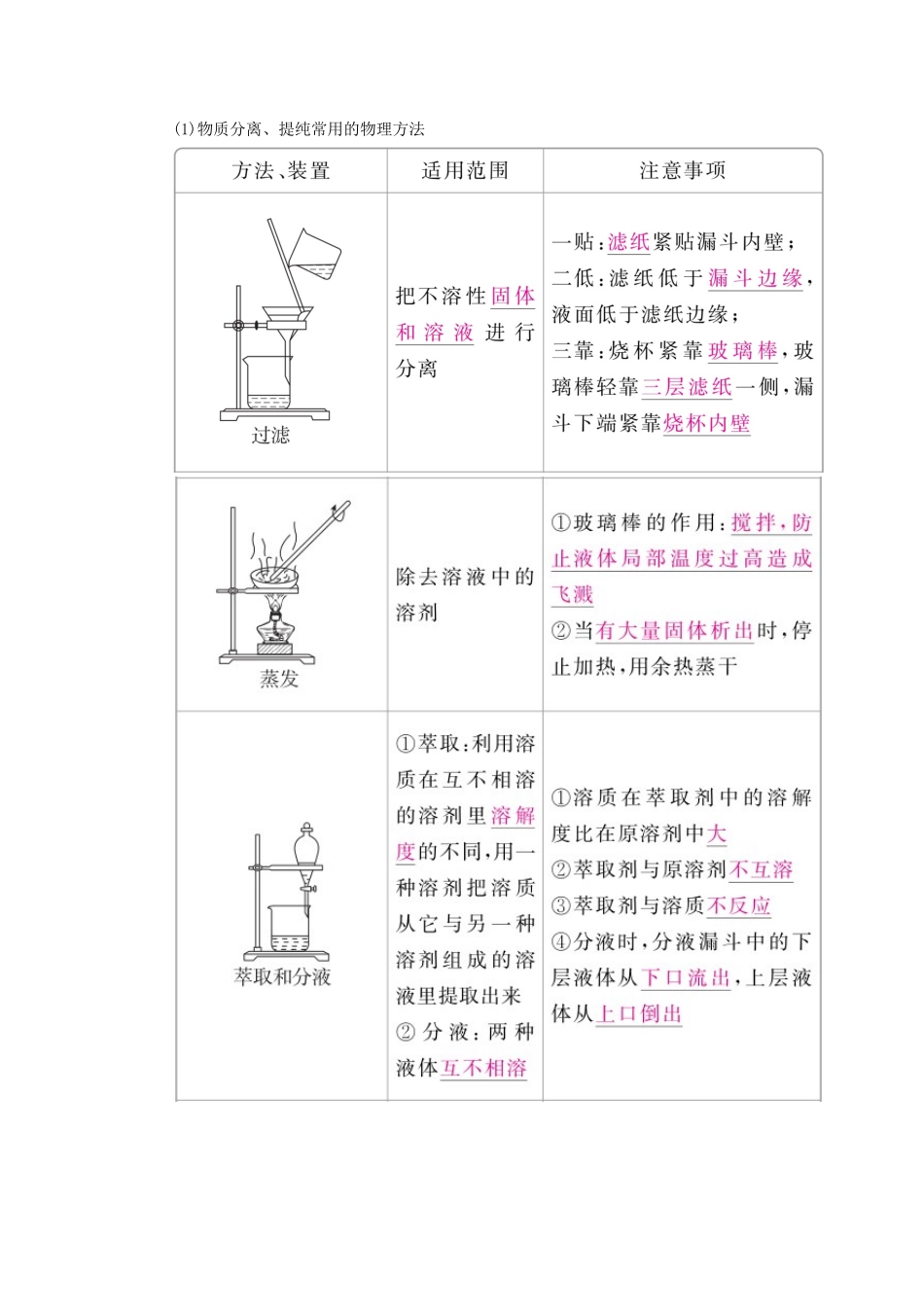
第 36 讲 物质的检验、分离和提纯1.物质的检验(1)常见阳离子的检验常见阳离子试剂或方法实验现象Na+焰色反应黄色火焰K+焰色反应紫色火焰(透过蓝色钴玻璃)Mg2+NaOH 溶液白色沉淀,不溶于过量的碱Al3+NaOH 溶液白色沉淀,溶于过量的强碱Fe2+①NaOH 溶液① 白色沉淀→灰绿色→红褐色② 先加 KSCN 溶液,再加氯水② 先无明显现象,再变血红色Fe3+①NaOH 溶液① 生成红褐色沉淀②KSCN 溶液② 溶液呈红色③ 苯酚溶液③ 溶液呈紫色Cu2+NaOH 溶液蓝色沉淀续表(2)常见阴离子的检验常见阴离子试剂或方法现象Cl-硝酸银溶液与稀 HNO3白色沉淀,不溶于稀硝酸Br-硝酸银溶液与稀 HNO3浅黄色沉淀,不溶于稀硝酸氯水和四氯化碳溶液分层,下层为橙红色续表(3)常见气体的检验气体检验方法有关反应的方程式或说明Cl2使湿润的淀粉碘化钾试纸变蓝2KI + Cl 2== =2KCl + I 2(淀粉遇 I2变蓝)NH3① 能使湿润的红色石蕊试纸变蓝② 用蘸浓盐酸的玻璃棒靠近,产生白烟①NH3+H2ONH3·H2ONH+OH-②NH3+HCl===NH4ClSO2使品红溶液褪色,加热,又变红色SO2有漂白性CO2① 能使燃着的木条熄灭② 能使澄清的石灰水变浑浊Ca2++2OH-+CO2=== CaCO3↓+H2ONO无色气体,在空气中变为红棕色2NO + O 2== =2NO 2NO2① 红棕色、有刺激性气味的气体② 能使湿润的蓝色石蕊试纸变红③ 溶于水后生成无色气体和无色溶液3NO2+ H 2O == =2HNO 3+ NO 2.物质的分离和提纯(1)物质分离、提纯常用的物理方法(2)物质分离、提纯常用的化学方法方法原理杂质成分沉淀法将杂质离子转化为沉淀Cl-、SO、CO、Ba2+、Ca2+、Fe3+、Ag+气化法将杂质离子转化为气体CO、HCO