第一单元原子核外电子排布与元素周期律第一课时原子核外电子的排布、元素周期律[课标要求]1.知道核外电子能量高低与分层排布的关系
2.能够根据核外电子排布规律写出常见简单原子的原子结构示意图
3.通过分析 1~18 号元素原子核外电子排布、原子半径、主要化合价的变化,总结出它们的递变规律,并由此认识元素周期律
4.初步认识元素性质的周期性变化是元素原子核外电子排布周期性变化的必然结果
原子核外电子排布规律的“1 个最低”和“3 个最多”:(1)“1 个最低”——核外电子总是尽量先排布在能量最低的电子层里;(2)“3 个最多”——①各电子层最多容纳电子数 2n2;②最外层电子数最多 8 个;③次外层电子数最多 18 个
2.原子中,原子序数=核电荷数=质子数=核外电子数
3.电子层数相同的元素,随着核电荷数的递增,金属性逐渐减弱,非金属性逐渐增强,即元素的性质,随着原子序数的递增,呈现周期性变化
4.微粒半径大小的变化规律(1)电子层数相同时,随原子序数的递增,原子半径逐渐减小;(2)最外层电子数相同时,随电子层数的递增,原子半径逐渐增大;(3)具有相同核外电子排布的离子,原子序数越大,离子半径越小
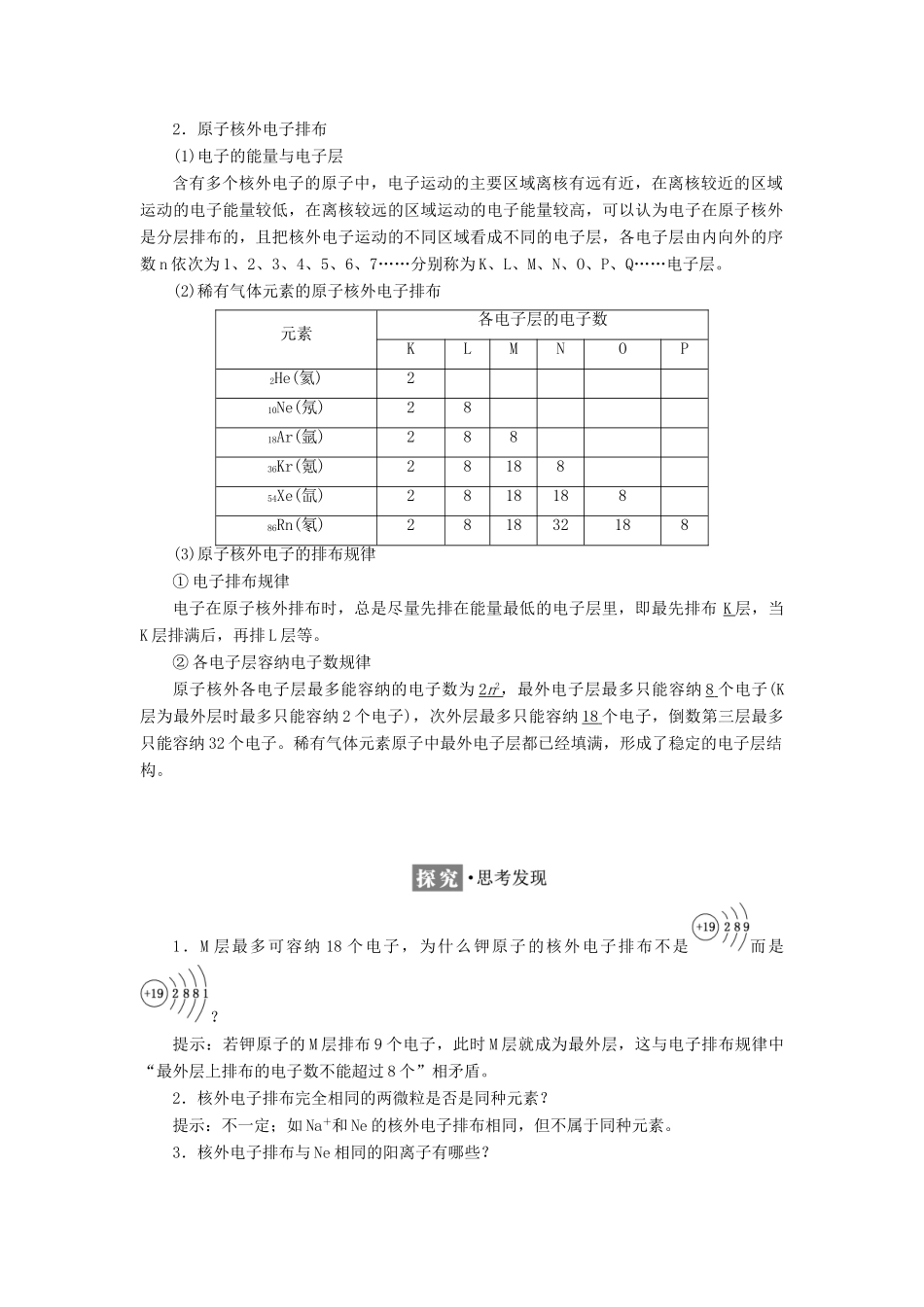
原子核外电子的排布1.原子结构(1)原子的构成(2)原子结构的表示方法——原子结构示意图(以钠原子为例) 2.原子核外电子排布(1)电子的能量与电子层含有多个核外电子的原子中,电子运动的主要区域离核有远有近,在离核较近的区域运动的电子能量较低,在离核较远的区域运动的电子能量较高,可以认为电子在原子核外是分层排布的,且把核外电子运动的不同区域看成不同的电子层,各电子层由内向外的序数 n 依次为 1、2、3、4、5、6、7……分别称为 K、L、M、N、O、P、Q……电子层
(2)稀有气体元素的原子核外电子排布元素各电子层的电子数KLMNOP2He(氦)210Ne(氖)2818A