第二课时 晶格能学习目标:了解晶体的晶格能,知道晶格能的大小可以衡量离子晶体中离子键的强弱,掌握离子键的强弱与离子半径以及离子所带的电荷的关系
[知识回顾]1.离子晶体的概念:由阳离子和阴离子通过离子键结合而成的晶体
2.决定离子晶体结构的因素有哪些
答:几何因素、电荷因素、键性因素
3.离子晶体的性质(1)硬度较大,难于压缩;(2)熔、沸点较高,难挥发;(3)不导电,但是在熔融态或水溶液中可导电
[要点梳理]晶格能(1)概念离子晶体的晶格能是指气态离子形成 1 _mol 离子晶体释放的能量 ,能量取正值
离子晶体的晶格能是最能反映离子晶体稳定性的数据
(2)影响因素离子带电荷越多,晶格能越大,离子半径越大,晶格能越小
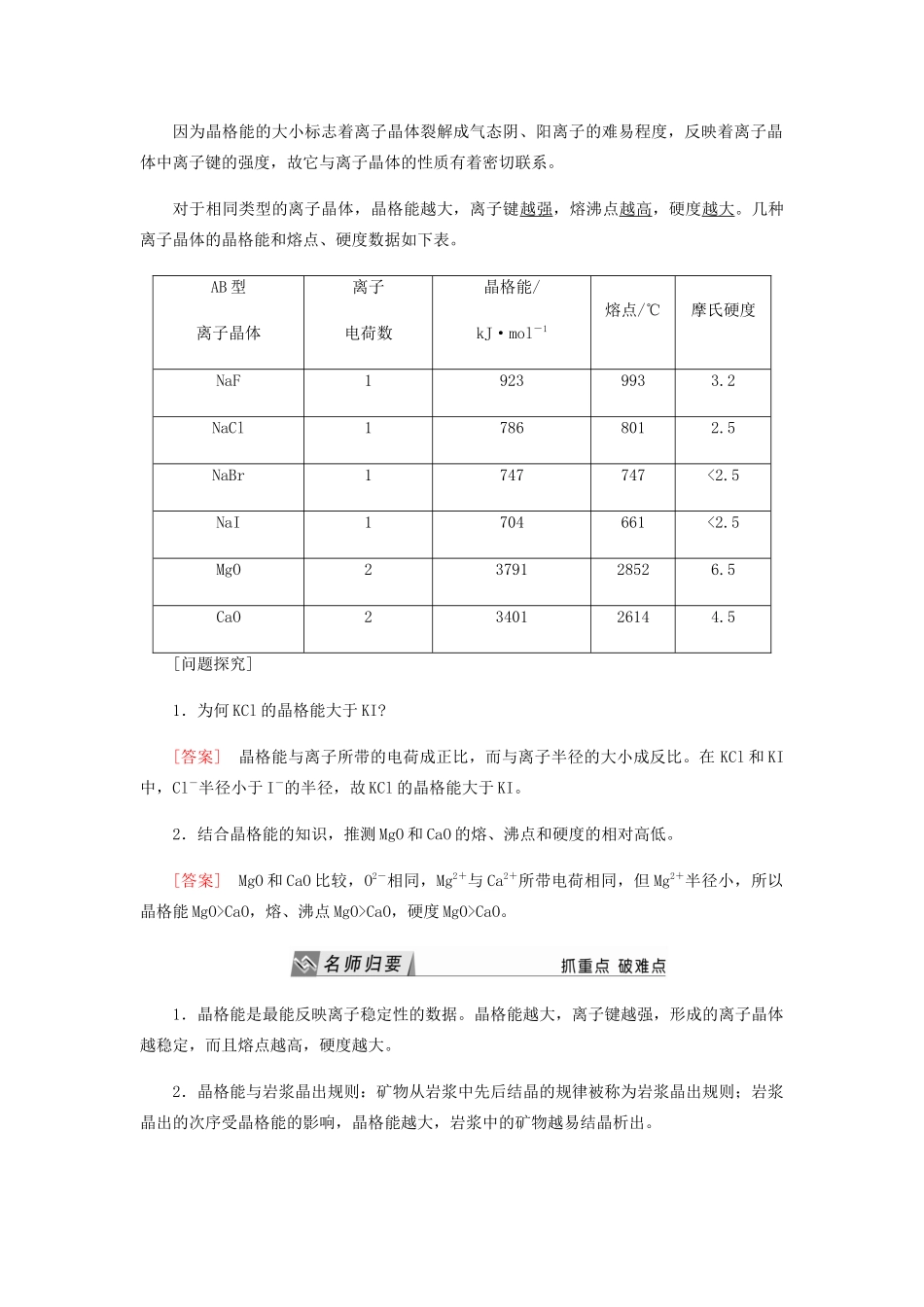
(3)晶格能对离子晶体性质的影响晶格能越大,形成的离子晶体越稳定,而且熔点越高,硬度越大
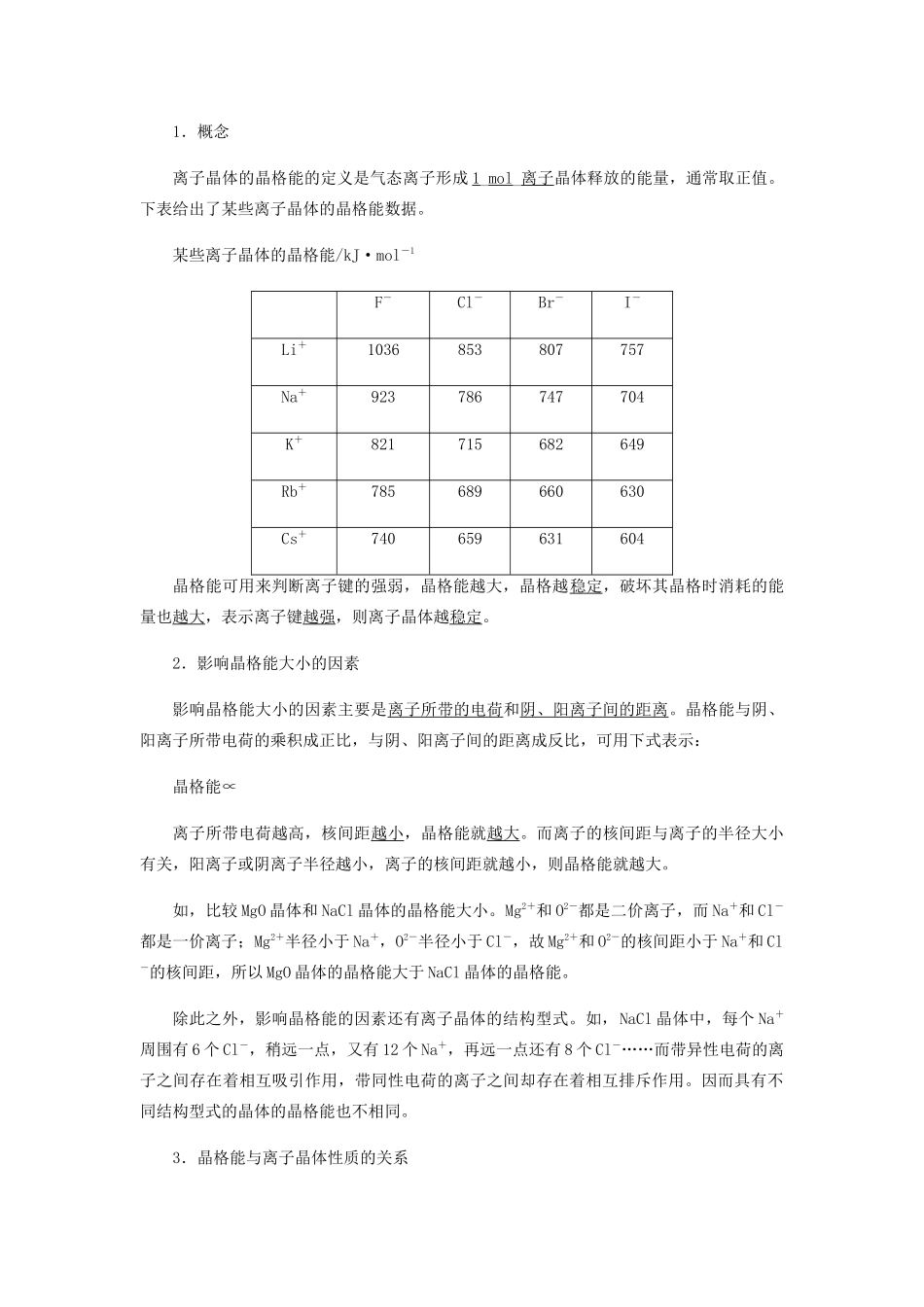
知识点 晶格能1.概念离子晶体的晶格能的定义是气态离子形成 1_mol_离子晶体释放的能量,通常取正值
下表给出了某些离子晶体的晶格能数据
某些离子晶体的晶格能/kJ·mol-1F-Cl-Br-I-Li+1036853807757Na+923786747704K+821715682649Rb+785689660630Cs+740659631604晶格能可用来判断离子键的强弱,晶格能越大,晶格越稳定,破坏其晶格时消耗的能量也越大,表示离子键越强,则离子晶体越稳定
2.影响晶格能大小的因素影响晶格能大小的因素主要是离子所带的电荷和阴、阳离子间的距离
晶格能与阴、阳离子所带电荷的乘积成正比,与阴、阳离子间的距离成反比,可用下式表示:晶格能∝离子所带电荷越高,核间距越小,晶格能就越大
而离子的核间距与离子的半径大小有关,阳离子或阴离子半径越小,离子的核间距就越小,则晶格能就越大
如,比较 MgO 晶体和 NaCl 晶体的晶格能大小
Mg2+和 O2-都是二价离子,而 Na+和