第一课时 共价键学习目标:1
知道化学键的概念,能用电子式表示常见物质的离子键或共价键的形成过程
知道共价键的主要类型 σ 键和 π 键
说出 σ 键和 π 键的明显差别和一般规律
[知识回顾]1.分子中相邻原子之间是靠什么作用而结合在一起
什么是化学键
什么是离子键
什么是共价键
答:分子中相邻原子之间是靠共价键而结合在一起
化学键:分子中相邻原子之间强烈的相互作用
离子键:阴、阳离子之间通过静电作用形成的化学键
共价键:原子间通过共用电子对形成的化学键
2.用电子式表示 NaCl、HCl 的形成过程
答:H·+·Cl∶―→H∶Cl∶[要点梳理]1.共价键的基本知识(1)概念:原子间通过共用电子对所形成的相互作用,叫做共价键
(2)成键的粒子:原子,一般为非金属原子(相同或不相同)或金属原子与非金属原子
(3)键的本质:原子间通过共用电子对(即电子云重叠)产生的强烈作用
(4)键的形成条件:非金属元素的原子之间形成共价键,大多数电负性之差小于 1
7 的金属与非金属元素的原子之间形成共价键
如 Al 原子与 F 原子变为 Al3+和 F-后形成离子键,Al 原子和 Cl 原子之间则形成共价键
(5) 存 在 : 共 价 键 存 在 于 非 金 属 单 质 、 共 价 化 合 物 和 某 些 离 子 化 合 物 中
如H2、Cl2、O2、S8、N2、P4、金刚石、晶体硅等非金属单质,CO2、H2O、CH3COOH、XeF6、等共价化合物及 Na2O2、NaOH、NH4Cl 等离子化合物中均存在共价键
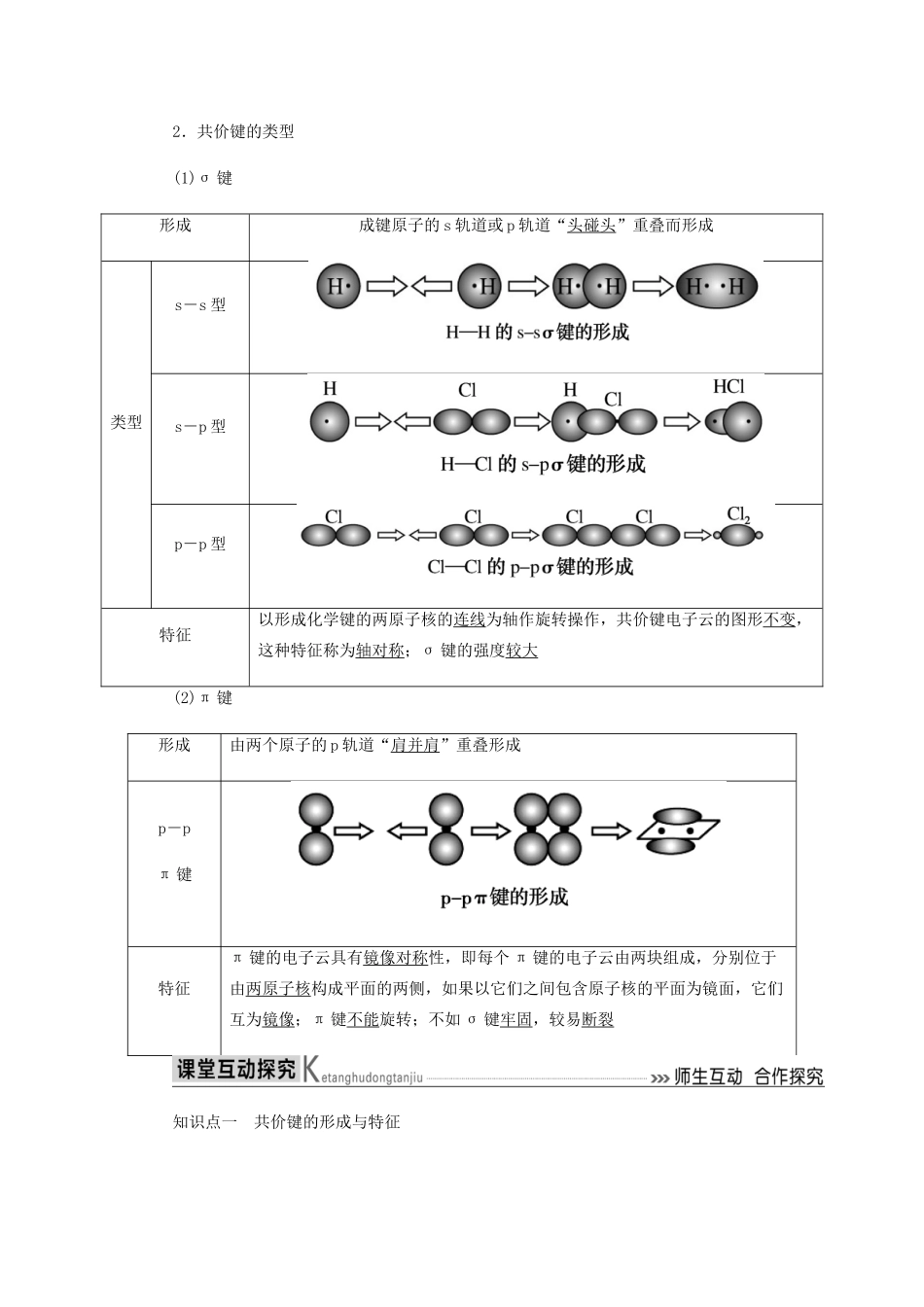
2.共价键的类型(1)σ 键形成成键原子的 s 轨道或 p 轨道“头碰头”重叠而形成类型s-s 型s-p 型p-p 型特征以形成化学键的两原子核的连线为轴作旋转操作,共价键电子云的图形不变,这种特征称为轴对称;σ 键的强度较大(2)π 键形成由两个原子的 p