第一课时 形形色色的分子 价层电子对互斥理论学习目标:1
认识共价分子结构的多样性和复杂性
能根据有关理论判断简单分子或离子的构型
能说明简单配合物的成键情况
[知识回顾]1.键能:气态基态原子形成 1 _mol 化学键释放的最低能量
键能越大,化学键越稳定
2.键长:形成共价键的两个原子之间的核间距
键长越短,键能越大,共价键越稳定
3.键角:在原子数超过 2 的分子中,两个共价键的夹角
键角是描述分子立体结构的重要参数
4.等电子体是指原子总数相等、价电子总数相同的微粒,其电子总数不一定相同
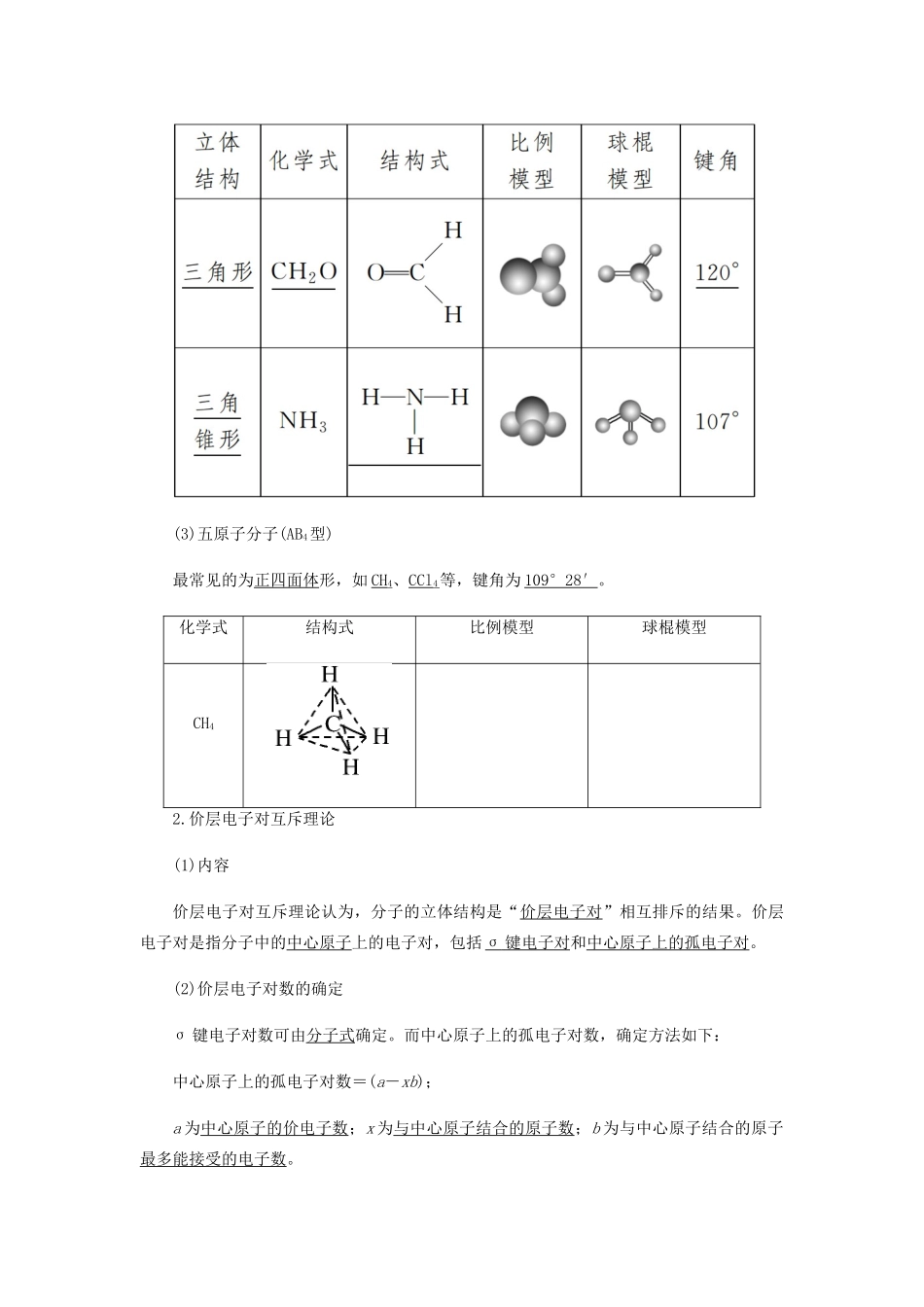
[要点梳理]1.形形色色的分子(1)三原子分子(AB2型)(2)四原子分子(AB3型)(3)五原子分子(AB4型)最常见的为正四面体形,如 CH4、CCl4 等,键角为 109°28′
化学式结构式比例模型球棍模型CH42
价层电子对互斥理论(1)内容价层电子对互斥理论认为,分子的立体结构是“价层电子对”相互排斥的结果
价层电子对是指分子中的中心原子上的电子对,包括 σ 键电子对 和中心原子上的孤电子对
(2)价层电子对数的确定σ 键电子对数可由分子式确定
而中心原子上的孤电子对数,确定方法如下:中心原子上的孤电子对数=(a-xb);a 为中心原子的价电子数;x 为与中心原子结合的原子数;b 为与中心原子结合的原子最多能接受的电子数
(3)VSEPR 模型和分子的立体结构H2O 的中心原子上有 2 对孤电子对,与中心原子上的 σ 键电子对相加等于 4,它们相互排斥形成四面体形 VSEPR 模型
略去 VSEPR 模型中的中心原子上的孤电子对,因而 H2O 的立体结构为 V 形
知识点一 常见分子的立体构型1.分子的键角和空间结构分子类型分子的立体结构键角A--A2直线(对称)形-AB直线(非对称)形-AB2或 A2BAB2直线(对称)形180°A2B折线(不对称)形