化学选修 3《第三章 晶体结构与性质》知识点总结一.晶体常识1.晶体与非晶体比较2.获得晶体的三条途径① 熔融态物质凝固
②气态物质冷却不经液态直接凝 固(凝华)
③溶质从溶液中析出
3.晶胞晶胞是描述晶体结构的基本单元
晶胞在晶体中的排列呈“无隙并置”
4.晶胞中微粒数的计算方法——均摊法如某个粒子为 n 个晶胞所共有,则该粒子有 1/n 属于这个晶胞
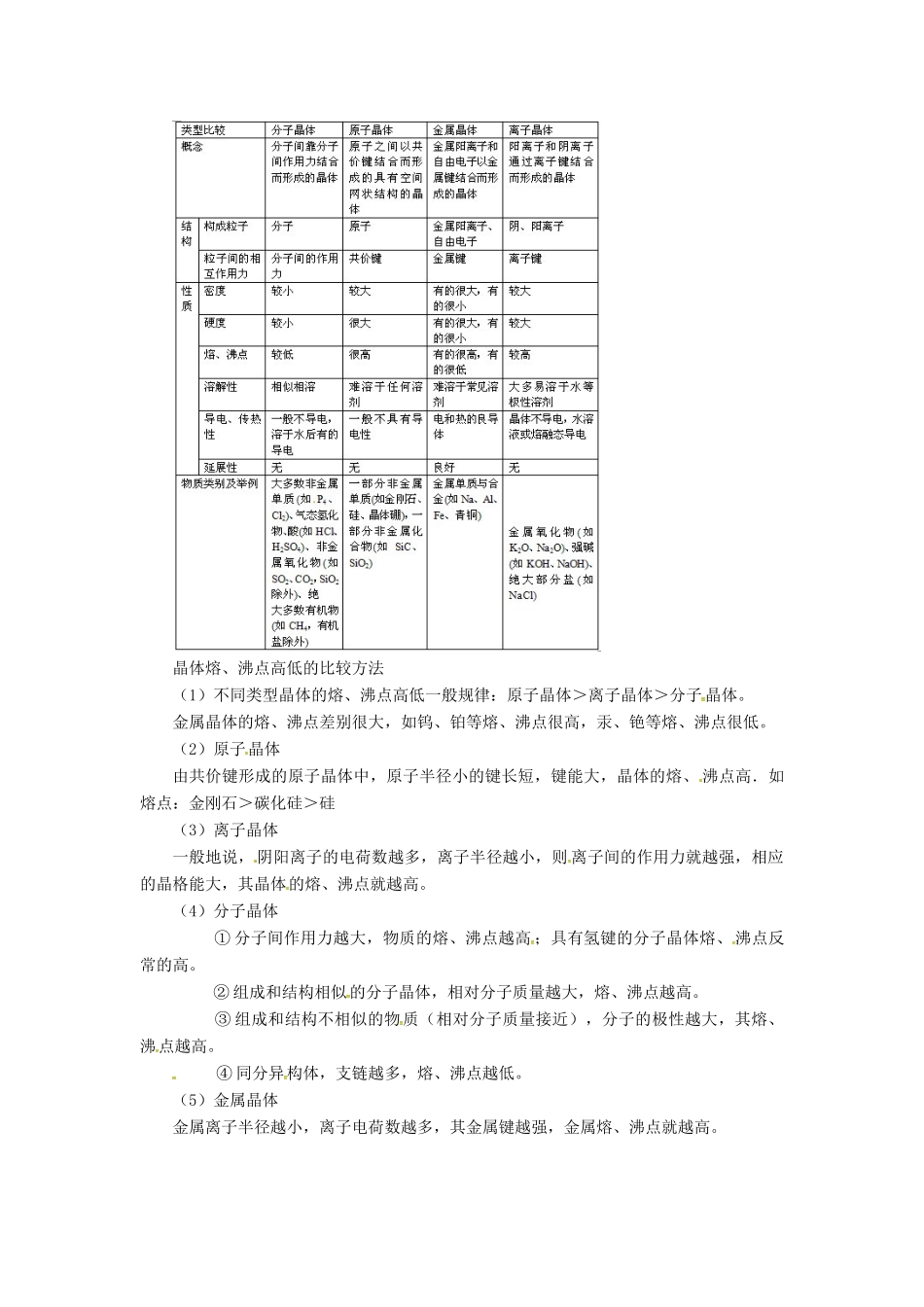
中学中常见的晶胞为立方晶胞立方晶胞中微粒数的计算方法如下:注意:在使用“均摊法”计算晶胞中粒子个数时要注意晶胞的形状二.四种晶体的比较晶体熔、沸点高低的比较方法(1)不同类型晶体的熔、沸点高低一般规律:原子晶体>离子晶体>分子 晶体
金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低
(2)原子晶体由共价键形成的原子晶体中,原子半径小的键长短,键能大,晶体的熔、 沸点高.如熔点:金刚石>碳化硅>硅 (3)离子晶体一般地说, 阴阳离子的电荷数越多,离子半径越小,则 离子间的作用力就越强,相应的晶格能大,其晶体的熔、沸点就越高
(4)分子晶体 ① 分子间作用力越大,物质的熔、沸点越高 ;具有氢键的分子晶体熔、 沸点反常的高
② 组成和结构相似 的分子晶体,相对分子质量越大,熔、沸点越高
③ 组成和结构不相似的物 质(相对分子质量接近),分子的极性越大,其熔、沸点越高
④ 同分异构体,支链越多,熔、沸点越低
(5)金属晶体金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高
三.几种典型的晶体模型