物质的制备和检验1 复习重点1.掌握常见气体的实验室制法(包括所用试剂、仪器、反应原理和收集方法).2.综合运用化学知识对常见的物质(包括气体物质、无机离子)进行分离、提纯和鉴别.难点聚焦一、常见气体的实验室制备1、气体发生装置的类型(1)设计原则:根据反应原理、反应物状态和反应所需条件等因素来选择反应装置
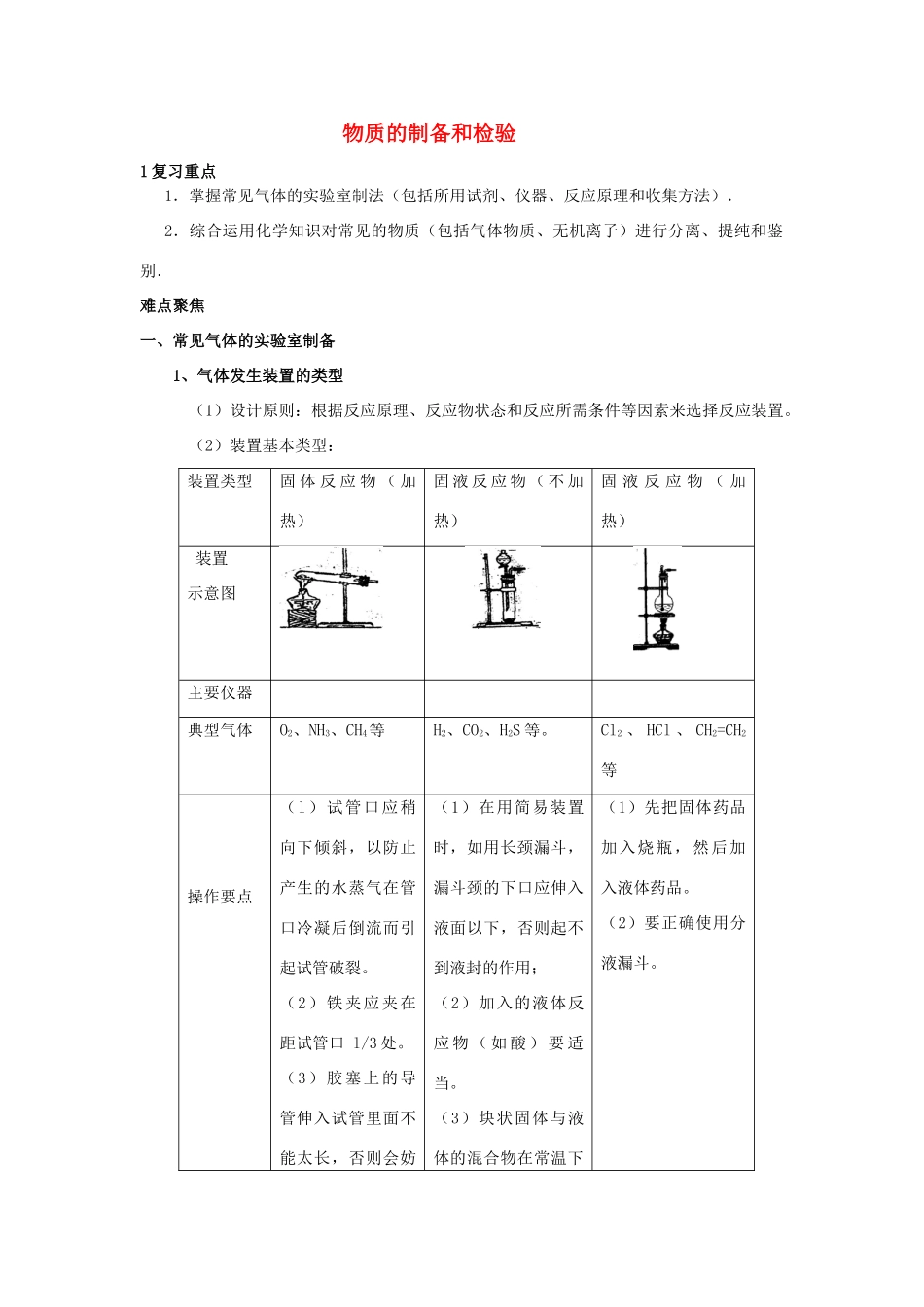
(2)装置基本类型:装置类型固 体 反 应 物 ( 加热)固 液 反 应 物 ( 不 加热)固 液 反 应 物 ( 加热) 装置示意图主要仪器典型气体O2、NH3、CH4等H2、CO2、H2S 等
Cl2 、 HCl 、 CH2=CH2等操作要点(l)试管口应稍向下倾斜,以防止产生的水蒸气在管口冷凝后倒流而引起试管破裂
(2)铁夹应夹在距试管口 l/3 处
(3)胶塞上的导管伸入试管里面不能太长,否则会妨(1)在用简易装置时,如用长颈漏斗,漏斗颈的下口应伸入液面以下,否则起不到液封的作用;(2)加入的液体反应 物 ( 如 酸 ) 要 适当
(3)块状固体与液体的混合物在常温下(1)先把固体药品加入烧瓶,然后加入液体药品
(2)要正确使用分液漏斗
碍气体的导出
反应制备气体可用启普发生器制备
几种气体制备的反应原理1、O2 2KClO3 2KCl+3O2↑ 2KMnO4K2MnO4+MnO2+O2↑ 2H2O22H2O+O2↑2、NH3 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O NH3·H2ONH3↑+H2O3、CH4 CH3COONa+NaOHNa2CO3+CH4↑4、H2 Zn+H2SO4(稀)=ZnSO4+H2↑5、CO2 CaCO3+2HCl=CaCl2+CO2↑+H2O6、H2S FeS+H2SO4(稀)=FeSO4+H2S↑7、SO2 Na2SO4+H2SO4(浓)=Na2SO4+SO2↑+H2O8、NO2 Cu+4HNO3(浓)=Cu(N