玻尔的原子模型 课 题18.4 玻尔的原子模型第 2 课时教学目标1.了解玻尔原子理论的主要内容
2.了解能级、能量量子化以及基态、激发态的概念
教学重难点玻尔原子理论的基本假设、玻尔理论对氢光谱的解释
教学流程\内容\板书关键点拨加工润色从玻尔的基本假设出发,运用经典电磁学和经典力学的理论,可以计算氢原子中电子的可能轨道半径和相应的能量
(1)氢原子的大小:氢原子的电子的各条可能轨道的半径 rn: rn=n2r1,r1代表第一条(离核最近的一条)可能轨道的半径 r1=0
53×10-10 m例:n=2, r2=2
12×10-10 m(2)氢原子的能级:①原子在各个定态时的能量值 En称为原子的能级
它对应电子在各条可能轨道上运动时的能量 En(包括动能和势能) En=E1/n2 n=1,2,3,······E1代表电子在第一条可能轨道上运动时的能量E1=-13
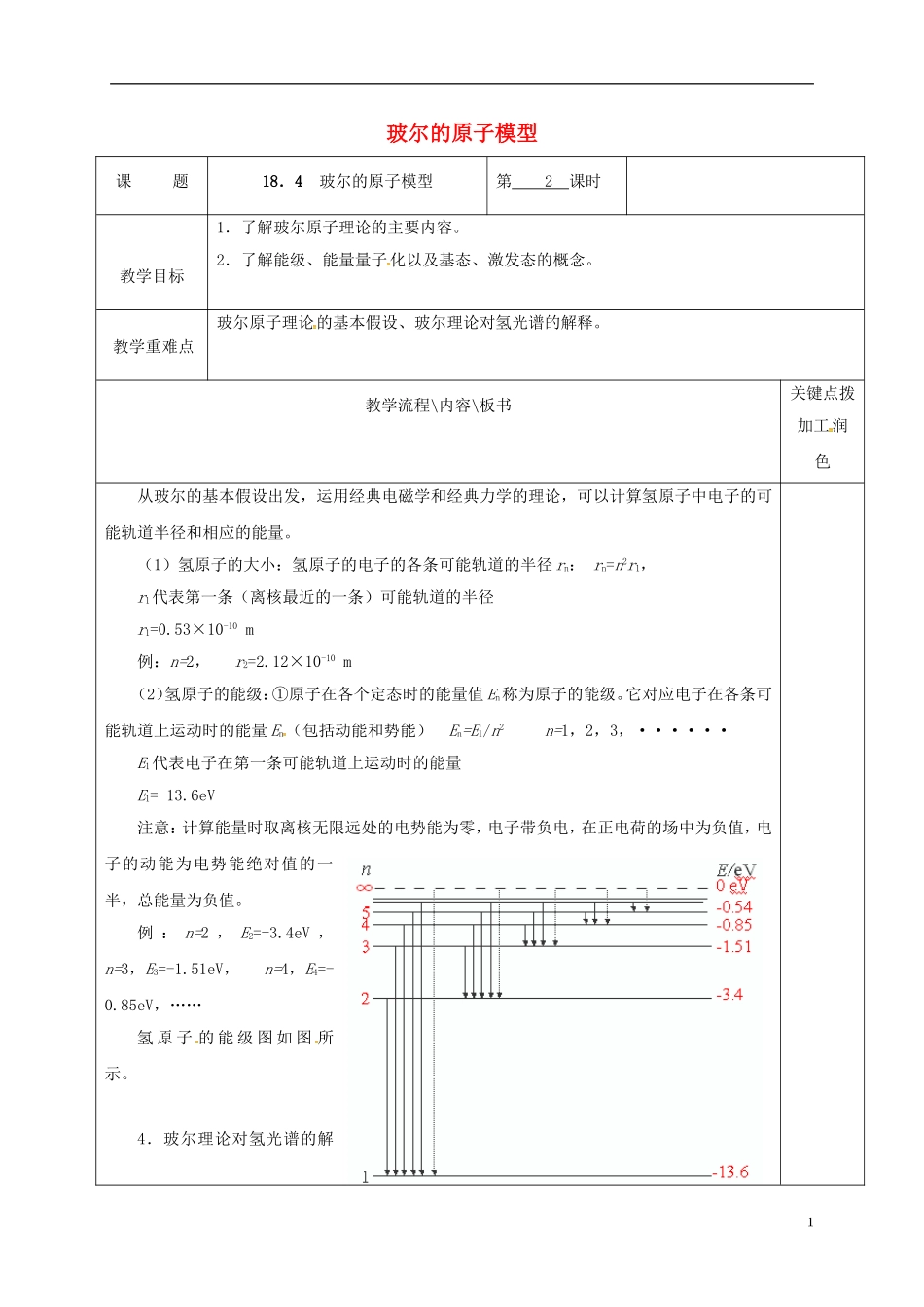
6eV 注意:计算能量时取离核无限远处的电势能为零,电子带负电,在正电荷的场中为负值,电子的动能为电势能绝对值的一半,总能量为负值
例 : n=2 , E2=-3
4eV , n=3,E3=-1
51eV, n=4,E4=-0
85eV,……氢 原 子 的 能 级 图 如 图 所示
4.玻尔理论对氢光谱的解1释(1)基态和激发态基态:在正常状态下,原子处于最低能级,这时电子在离核最近的轨道上运动,这种定态,叫基态
激发态:原子处于较高能级时,电子在离核较远的轨道上运动,这种定态,叫激发态
(2)原子发光:原子从基态向激发态跃迁的过程是吸收能量的过程
原子从较高的激发态向较低的激发态或基态跃迁的过程,是辐射能量的过程,这个能量以光子的形式辐射出去,吸收或辐射的能量恰等于发生跃迁的两能级之差
(三)课堂练习1.对玻尔理论的下列说法中,正确的是( ACD )A.继承了卢瑟福的原子模型,但对原子能量和电子轨道引入了量子化