中和反应及其应用1
氢氧化钠 NaOH 易溶 ;氢氧化铁 Fe(OH)3 不溶(红褐色);氢氧化钙 Ca(OH)2 微溶;氢氧化铜 Cu(OH)2 不溶(蓝色)
2 .写出下列反应的化学方程式:(1)Cu(OH)2+2HCl==CuCl2+2H2O ;(2)2Fe(OH)3+3H2SO4==Fe2(SO4)3+6H2O ;(3)NaOH+HCl==NaCl+H2O
3 .什么叫中和反应
酸和碱各自的特性都消失,生成了盐和水的反应
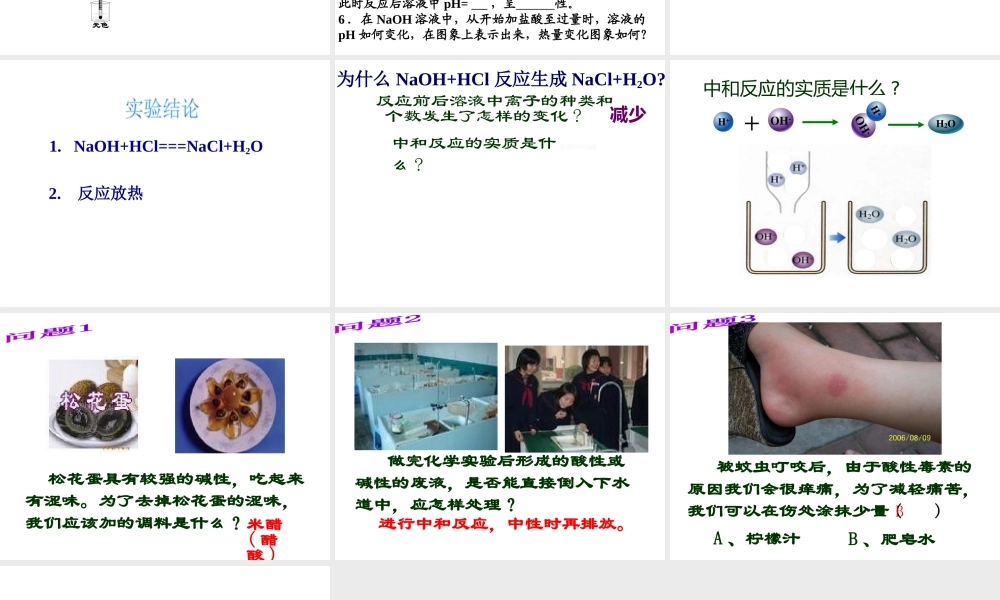
中和反应的实质是什么
H++OH-==H2O
4 .中和反应的应用有:( 1 )改良酸性土壤;( 2 )处理工厂废水中的酸;( 3 )用于医药——中和胃酸及昆虫分泌的酸性物质等;( 4 )蚊虫叮咬的止痛、消肿
你发现了什么问题
氢氧化钠溶液盐酸溶液【实验 1 】在烧杯中加入氢氧化钠溶液 10mL ,滴加 2~3 滴酚酞试液,插入一支温度计,测量溶液的温度
酚酞溶液10mL 氢氧化钠溶液酚酞 +氢氧化钠溶液温度
用胶头滴管吸取稀盐酸逐滴加入氢氧化钠溶液中,边加边搅拌,观察现象,滴到刚好褪色,停止滴入稀盐酸,用温度计再测量溶液温度
无色稀盐酸红色 温度怎样变化
1 .在上述实验中溶液的碱性发生了什么变化
,这说明了什么
; 2 .在该反应中加入酚酞试液的作用是什么
; 3 .在实验中盐酸为什么逐滴滴入
; 4 .在反应中边滴加边振荡的作用是什么
;5 .何时反应刚好完成
此时反应后溶液中 pH= ,呈 性
6 .在 NaOH 溶液中,从开始加盐酸至过量时,溶液的pH 如何变化,在图象上表示出来,热量变化图象如何
为什么要返滴一滴
【实验 2 】 : 向【实验 1 】后所得的溶液中,用另一支胶头滴管滴加 1 滴氢氧化钠溶液,观察颜色
证明稀盐酸和氢氧化钠发生了反应而不是酸和酚酞反应证明稀盐酸和氢氧化钠完全反应