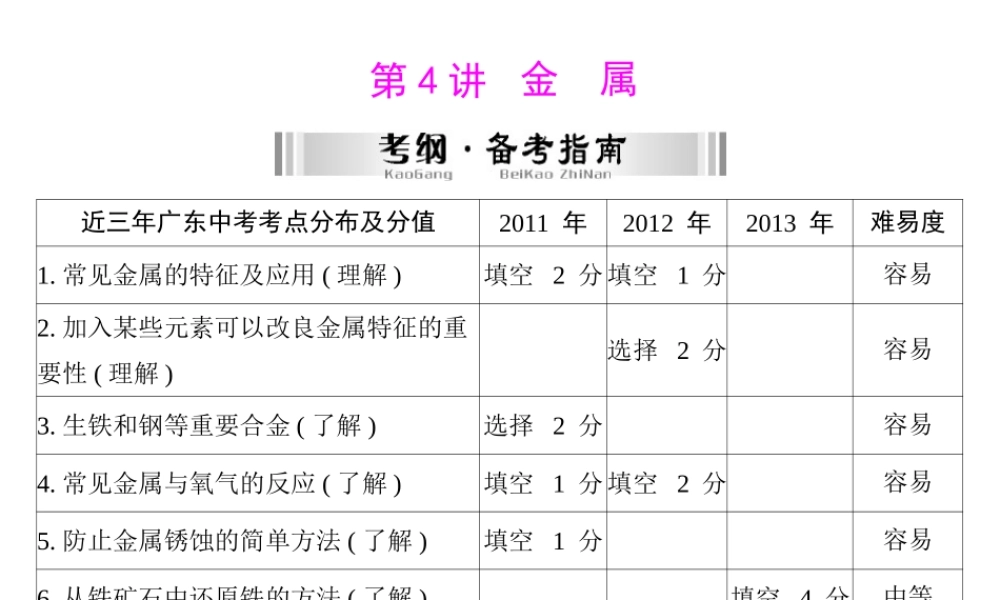
近三年广东中考考点分布及分值2011 年2012 年2013 年难易度1
常见金属的特征及应用 ( 理解 )填空 2 分填空 1 分容易2
加入某些元素可以改良金属特征的重要性 ( 理解 )选择 2 分容易3
生铁和钢等重要合金 ( 了解 )选择 2 分容易4
常见金属与氧气的反应 ( 了解 )填空 1 分填空 2 分容易5
防止金属锈蚀的简单方法 ( 了解 )填空 1 分容易6
从铁矿石中还原铁的方法 ( 了解 )填空 4 分中等7
用金属活动性顺序对有关置换反应进行简单的判断 ( 理解 )填空 1 分填空 1 分选择 2 分较难第 4 讲金属考点一金属的物理性质1 .金属有共同的物理性质(1) 金属大多都有 ________ 光泽 ( 一般为银白色,铜为亮红色,金为金黄色 )
(2) 导 ________ 性
(3) 导 ________ 性
(4)________ 性 ( 能被拉伸或展开 )
金属电热延展2 .金属的用途物质的性质在很大程度上决定了其用途
考点二合金性质1 .合金的定义在金属中加热熔合某些 ________( 或 ________) 形成的具有金属特性的 ________
2 .合金的性能(1) 合金的硬度一般比组成它的纯金属要大;(2) 合金的熔点比组成它的纯金属要低
金属非金属混合物3 .常见重要合金(1) 铁合金包括 ________ 和 ________
(2) 不锈钢是铁和 ________ 、 ________ 等的合金
(3) 钛和钛合金被认为是 21 世纪的重要金属材料
它们具有的优良性能有熔点高、密度小、可塑性好、易于加工、机械性能好等,尤其是 ______________ 非常好
温馨提示合金属于金属材料而不是合成材料
生铁钢铬镍抗腐蚀性能3Fe+2O2Fe3O4 2Al+3CuSO4===Al2(SO4)3+