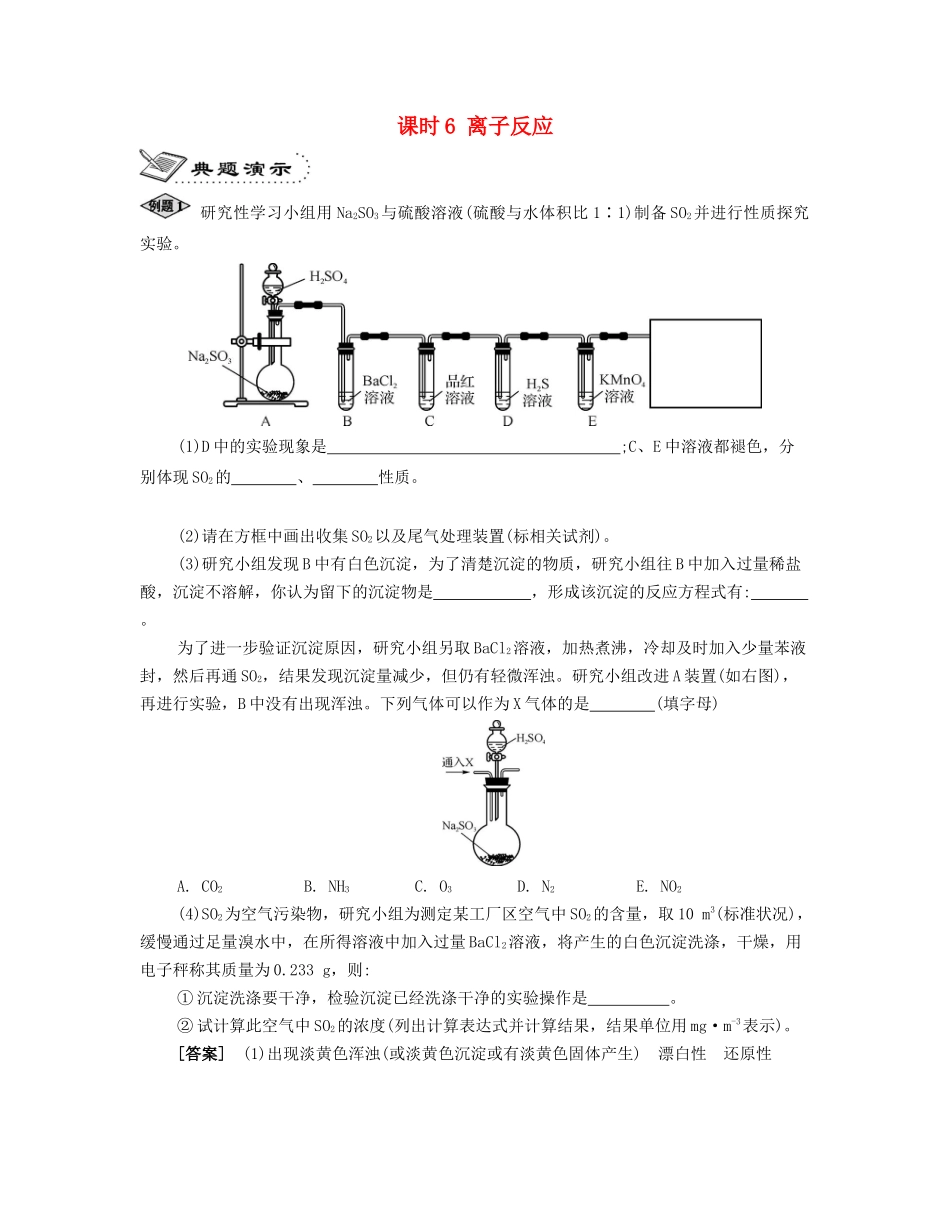
课时6离子反应研究性学习小组用Na2SO3与硫酸溶液(硫酸与水体积比1∶1)制备SO2并进行性质探究实验
(1)D中的实验现象是;C、E中溶液都褪色,分别体现SO2的、性质
(2)请在方框中画出收集SO2以及尾气处理装置(标相关试剂)
(3)研究小组发现B中有白色沉淀,为了清楚沉淀的物质,研究小组往B中加入过量稀盐酸,沉淀不溶解,你认为留下的沉淀物是,形成该沉淀的反应方程式有:
为了进一步验证沉淀原因,研究小组另取BaCl2溶液,加热煮沸,冷却及时加入少量苯液封,然后再通SO2,结果发现沉淀量减少,但仍有轻微浑浊
研究小组改进A装置(如右图),再进行实验,B中没有出现浑浊
下列气体可以作为X气体的是(填字母)A
NO2(4)SO2为空气污染物,研究小组为测定某工厂区空气中SO2的含量,取10m3(标准状况),缓慢通过足量溴水中,在所得溶液中加入过量BaCl2溶液,将产生的白色沉淀洗涤,干燥,用电子秤称其质量为0
233g,则:①沉淀洗涤要干净,检验沉淀已经洗涤干净的实验操作是
②试计算此空气中SO2的浓度(列出计算表达式并计算结果,结果单位用mg·m-3表示)
[答案](1)出现淡黄色浑浊(或淡黄色沉淀或有淡黄色固体产生)漂白性还原性(2)(3)BaSO4SO2+H2OH2SO3、2H2SO3+O22H2SO4、H2SO4+BaCl2BaSO4↓+2HClAD(4)①取最后一次洗涤液少量于试管中,加入硝酸酸化的AgNO3溶液,没有明显现象,证明洗涤干净②6
4mg·m-3[解析](1)SO2+2H2S3S↓+2H2O,有S生成,出现淡黄色浑浊;SO2使品红溶液褪色,体现了漂白性,而使高锰酸钾溶液褪色,说明SO2具有还原性
(2)SO2为有毒气体,应该进行尾气处理,用NaOH溶液吸收,注意防止倒吸
(3)SO2与水反应生成了亚硫酸,亚硫酸被