课时22原电池及其应用能力摸底课前热身1
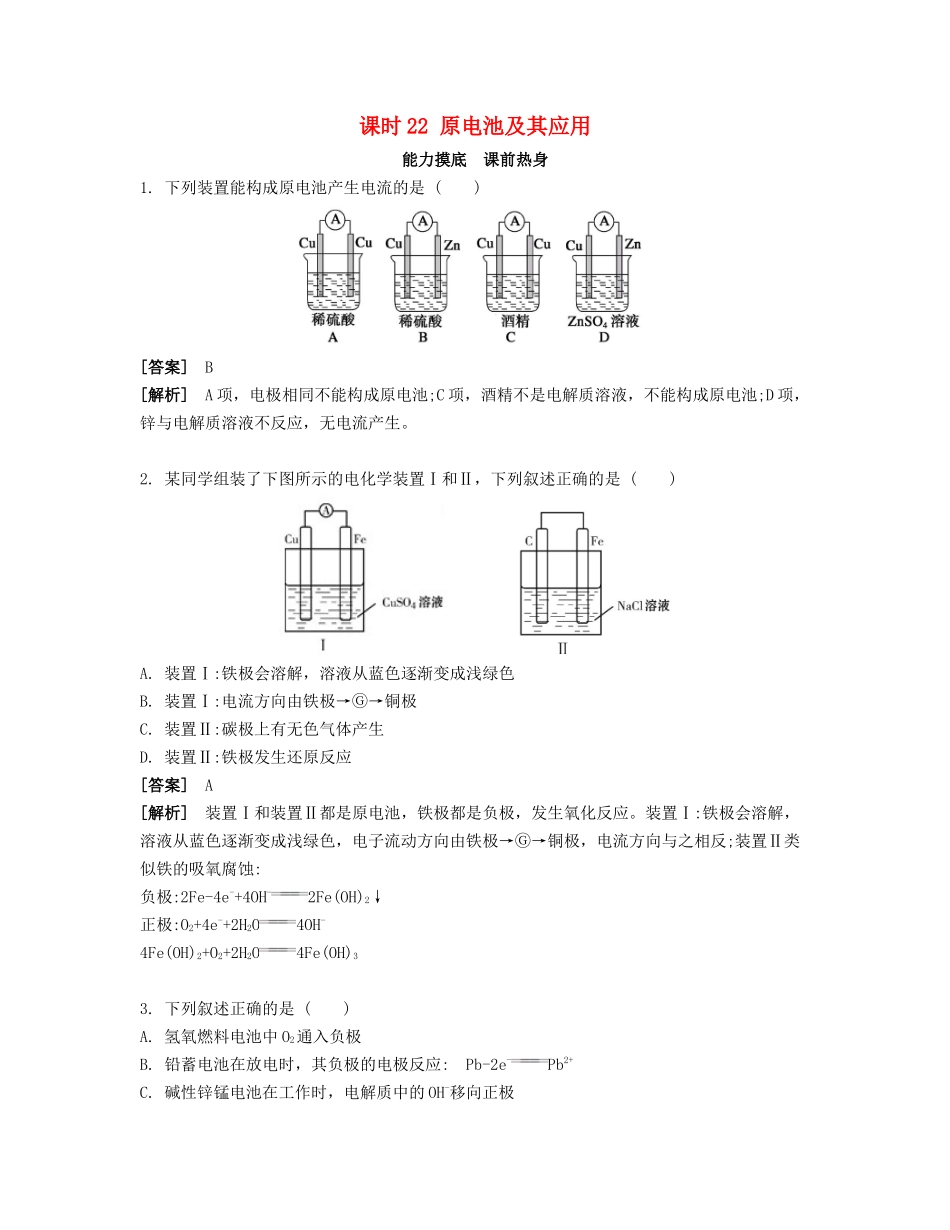
下列装置能构成原电池产生电流的是()[答案]B[解析]A项,电极相同不能构成原电池;C项,酒精不是电解质溶液,不能构成原电池;D项,锌与电解质溶液不反应,无电流产生
某同学组装了下图所示的电化学装置Ⅰ和Ⅱ,下列叙述正确的是()A
装置Ⅰ:铁极会溶解,溶液从蓝色逐渐变成浅绿色B
装置Ⅰ:电流方向由铁极→Ⓖ→铜极C
装置Ⅱ:碳极上有无色气体产生D
装置Ⅱ:铁极发生还原反应[答案]A[解析]装置Ⅰ和装置Ⅱ都是原电池,铁极都是负极,发生氧化反应
装置Ⅰ:铁极会溶解,溶液从蓝色逐渐变成浅绿色,电子流动方向由铁极→Ⓖ→铜极,电流方向与之相反;装置Ⅱ类似铁的吸氧腐蚀:负极:2Fe-4e-+4OH-2Fe(OH)2↓正极:O2+4e-+2H2O4OH-4Fe(OH)2+O2+2H2O4Fe(OH)33
下列叙述正确的是()A
氢氧燃料电池中O2通入负极B
铅蓄电池在放电时,其负极的电极反应:Pb-2e-Pb2+C
碱性锌锰电池在工作时,电解质中的OH-移向正极D
在海轮外壳镶嵌锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法[答案]D[解析]氢氧燃料电池中O2通入正极;铅蓄电池在放电时,其负极的电极反应为Pb(s)+S-2e-PbSO4(s);碱性锌锰电池在工作时,电解质中的OH-移向负极
(2014·新课标全国卷Ⅱ)2013年3月我国科学家报道了如下图所示的水溶液锂离子电池体系
下列叙述错误的是()A
a为电池的正极B
电池充电反应为LiMn2O4Li1-xMn2O4+xLiC
放电时,a极锂的化合价发生变化D
放电时,溶液中Li+从b向a迁移[答案]C[解析]根据题给装置图判断,Li金属电极b电极为原电池的负极,电极反应式为Li-e-Li+,则a为电池的正极,A项正确;a电极的电极反应式为Li1-xMn2O4+xLi+LiMn2O4,则