第二讲化学平衡状态化学平衡常数、化学反应进行的方向一、选择题1.已知:CaCO3(s)===CaO(s)+CO2(g)ΔH>0,ΔS>0,则该反应能自发进行的条件是()A.低温B.高温C.任何温度下都能自发进行D.任何温度下都不能自发进行解析ΔG=ΔH-TΔS<0时,反应能自发进行,因ΔH>0,ΔS>0,则在高温下ΔG可能小于零,故选B
答案B2.下列关于ΔH-TΔS说法中正确的是()A.ΔH-TΔS可用于判断所有条件下的反应能否自发进行B.ΔH-TΔS只用于判断温度、体积一定的反应能否自发进行C.ΔH-TΔS只用于判断温度、压强一定的反应能否自发进行D.ΔH-TΔS<0的反应,在该条件下一定剧烈反应解析在不同温度、压强下ΔH-TΔS的值不同,所以选项A、B都不正确;ΔH-TΔS<0能判定反应可以自发进行,但不一定是剧烈反应,所以答案为C
答案C3.25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示
下列判断正确的是()A.往平衡体系中加入金属铅后,c(Pb2+)增大B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小C.升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0D.25℃时,该反应的平衡常数K=2
2解析由于固体量改变不会引起平衡的移动,A项错误;加入固体Sn(NO3)2后,溶液中c(Sn2+)增大,平衡向左移动,从而使c(Pb2+)增大,B项错误;升高温度时c(Pb2+)增大,表明平衡向左移动,逆反应吸热,正反应的ΔH<0,C项错误;由图像中平衡时两种离子的浓度及平衡常数表达式知,25℃时该反应的平衡常数为2
2,D项正确
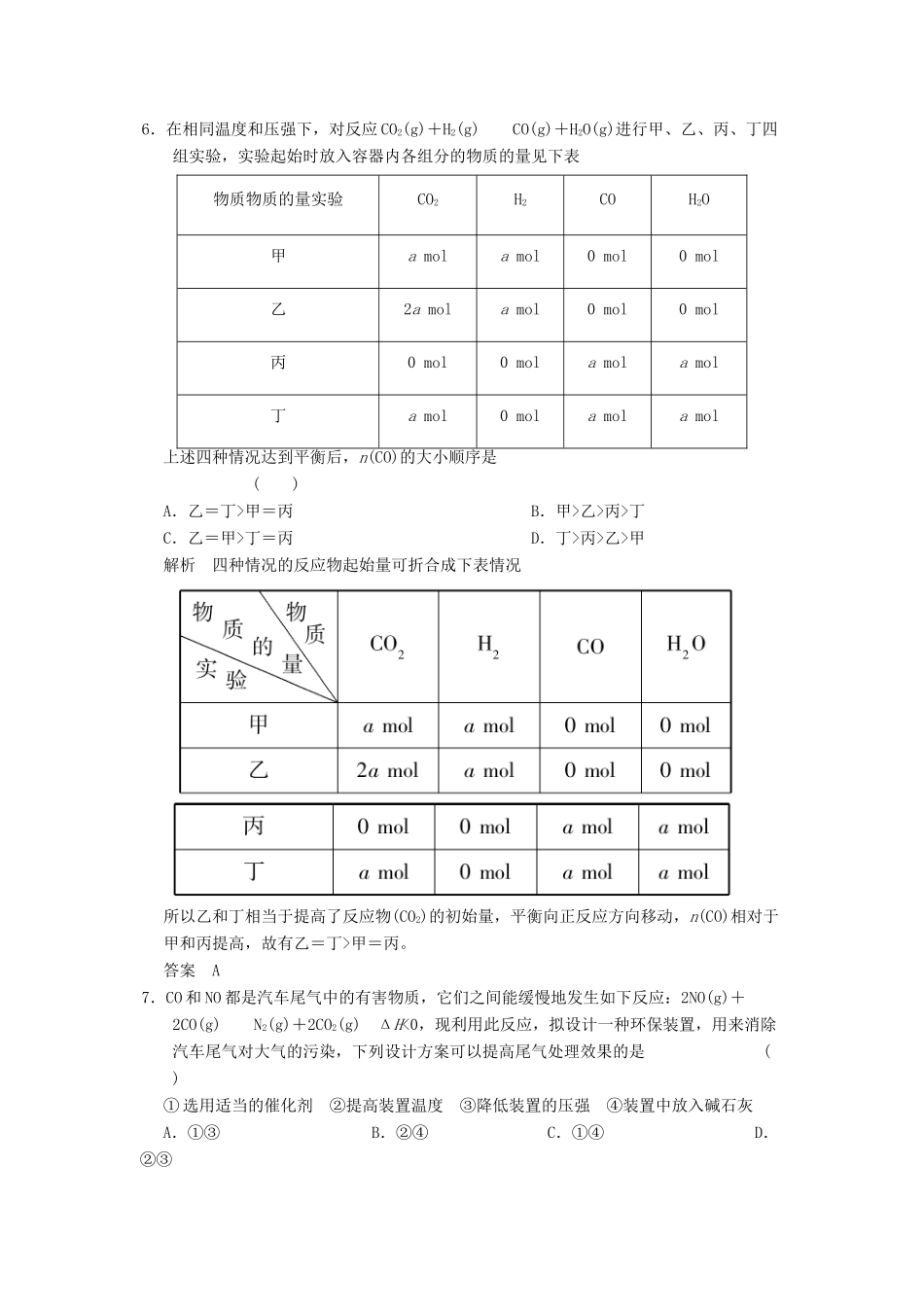
答案D4.在一定条件下,已达平衡的可逆反应:2A(g)+B(g)2C(g),