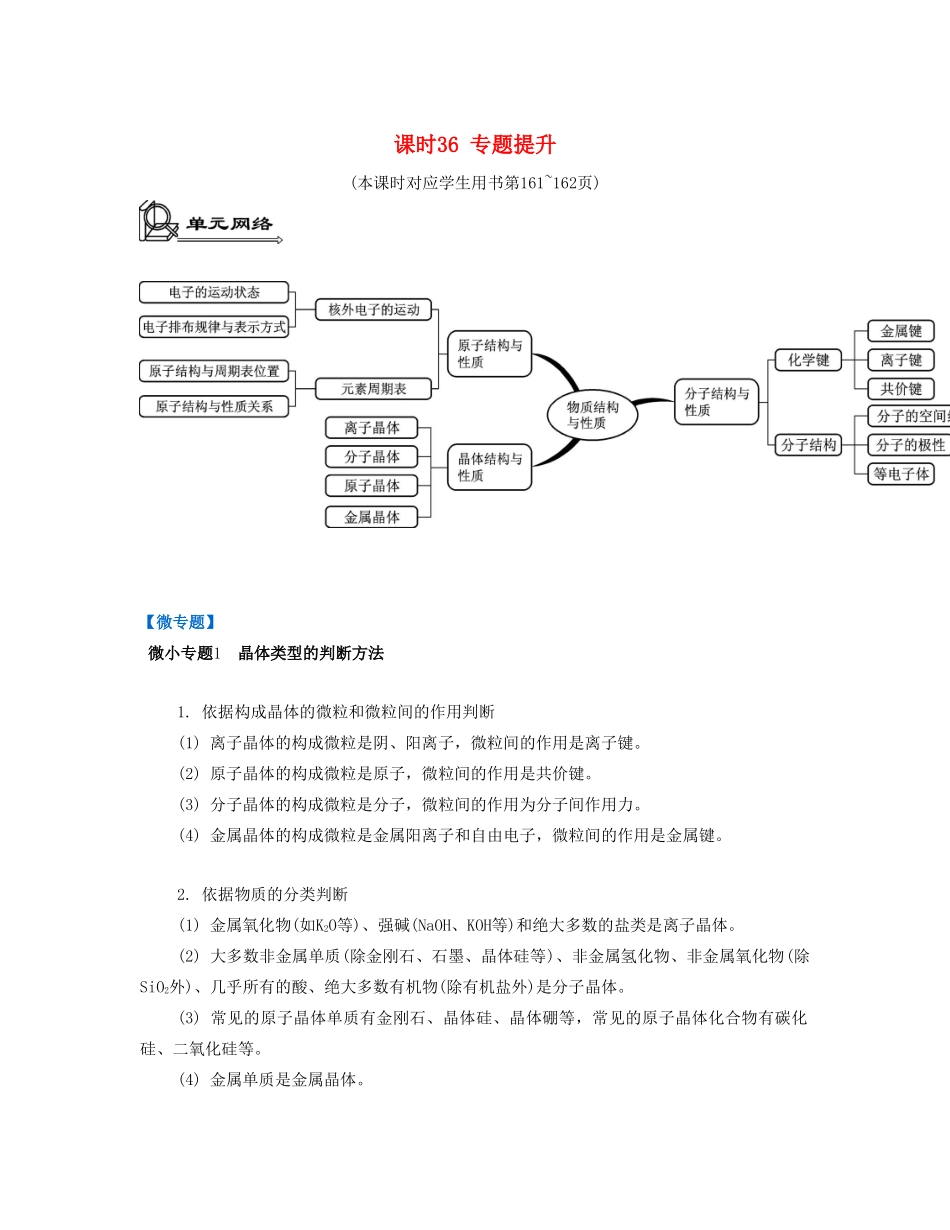
课时36专题提升(本课时对应学生用书第161~162页)【微专题】微小专题1晶体类型的判断方法1
依据构成晶体的微粒和微粒间的作用判断(1)离子晶体的构成微粒是阴、阳离子,微粒间的作用是离子键
(2)原子晶体的构成微粒是原子,微粒间的作用是共价键
(3)分子晶体的构成微粒是分子,微粒间的作用为分子间作用力
(4)金属晶体的构成微粒是金属阳离子和自由电子,微粒间的作用是金属键
依据物质的分类判断(1)金属氧化物(如K2O等)、强碱(NaOH、KOH等)和绝大多数的盐类是离子晶体
(2)大多数非金属单质(除金刚石、石墨、晶体硅等)、非金属氢化物、非金属氧化物(除SiO2外)、几乎所有的酸、绝大多数有机物(除有机盐外)是分子晶体
(3)常见的原子晶体单质有金刚石、晶体硅、晶体硼等,常见的原子晶体化合物有碳化硅、二氧化硅等
(4)金属单质是金属晶体
依据晶体的熔点判断(1)离子晶体的熔点较高,常在数百至一千摄氏度
(2)原子晶体的熔点高,常在一千摄氏度至几千摄氏度
(3)分子晶体的熔点低,常在数百摄氏度以下至很低温度
(4)金属晶体多数熔点高,但也有相当低的
依据导电性判断(1)离子晶体溶于水形成的溶液及熔融状态时能导电
(2)原子晶体一般为非导体
(3)分子晶体为非导体,而分子晶体中的电解质(主要是酸和强极性非金属氢化物)溶于水,使分子内的化学键断裂形成自由移动的离子,也能导电
(4)金属晶体是电的良导体
依据硬度和机械性能判断离子晶体硬度较大且脆
原子晶体硬度大
分子晶体硬度小且较脆
金属晶体多数硬度大,但也有较低的,且具有延展性
微小专题2物质的熔、沸点高低的比较方法1
不同类型晶体的熔、沸点高低,存在一般规律:原子晶体>离子晶体>分子晶体
金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低
原子晶体:由共价键形成的原子晶体中,原子半