第一章第三节化学键(第1课时)[教学目标]1.掌握离子键的概念
2.掌握离子键的形成过程和形成条件,并能熟练地用电子式表示离子化合物的形成过程
[教学重点]:离子键和离子化合物的概念[教学难点]:用电子式表示离子化合物的形成过程
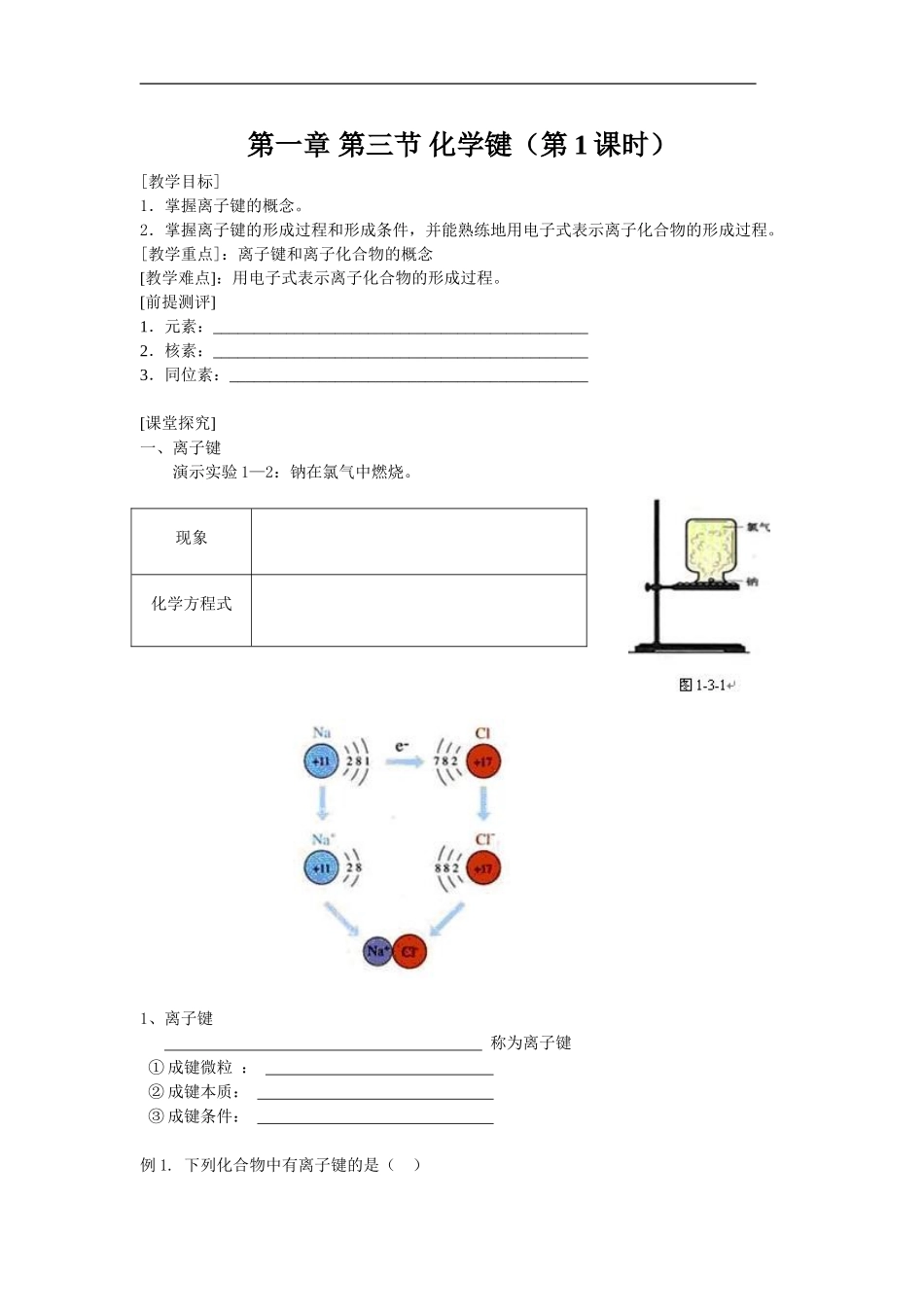
[前提测评]1.元素:______________________________________________2.核素:______________________________________________3.同位素:____________________________________________[课堂探究]一、离子键演示实验1—2:钠在氯气中燃烧
现象化学方程式1、离子键称为离子键①成键微粒:②成键本质:③成键条件:例1
下列化合物中有离子键的是()(1)AlCl3(2)HBr(3)Na2SO4(4)NH4Cl(5)H2CO32
结论:①__________________________________________________________________②__________________________________________________________________③__________________________________________________________________二、电子式1.电子式:在化学反应中,一般是原子的电子发生变化,我们可以在元素符号周围用小黑点(·或X)来代表原子的最外层电子,这种式子叫电子式
书写方式:①原子电子式:②离子的电子式:单核阳离子的电子式一般是离子符号本身,而阴离子的电子式要用方括号括起来
如Na+Mg2+③原子团电子式:如NH4+_________④离子化合物的电子式:如NaCl______例2用电子式表示原子或离子:氟原子钙原子氟