第三节化学键思考:1
为什么元素只有一百多种,却能形成二千多万种化合物,原子之间是怎样结合的
概念要点:a
强烈作用——相邻的原子之间强烈的相互作用2
化学键主要类型:a
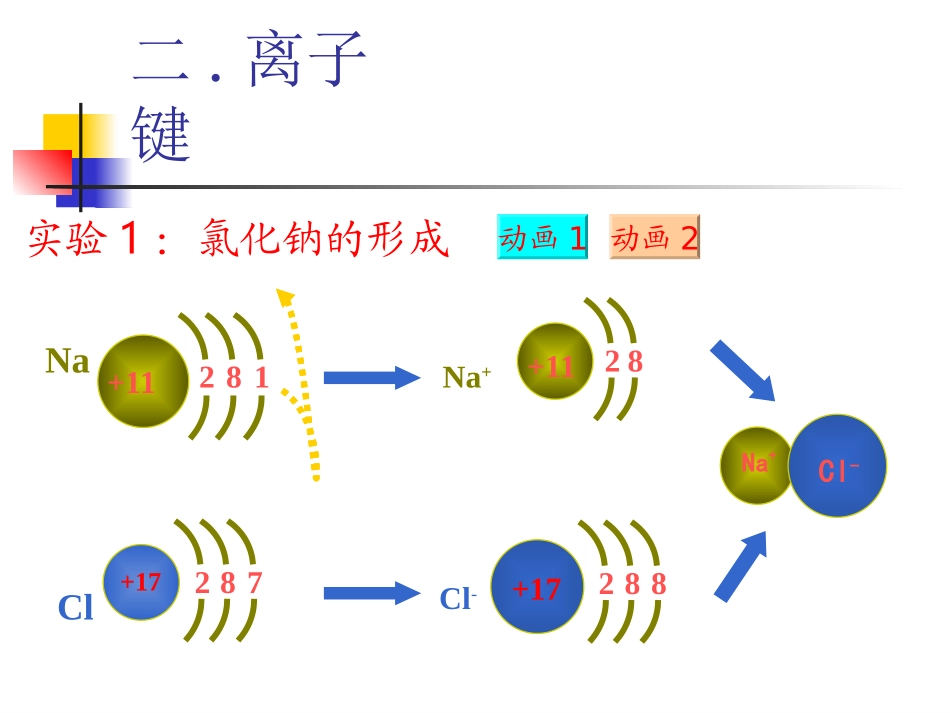
离子键实验1:氯化钠的形成动画1动画2Na+11812Cl+17872Na+Cl-+1182+17882Na+Cl-1
概念:阴阳离子间通过静电作用所形成的化学键2
概念要点:成键微粒——阴阳离子键的实质——静电作用成键范围——活泼金属(IAIIA)与非金属(VIAVIIA)思考题二
离子键原子:离子:ClNaNaO2-NaClMg2ClHOClMgNa离子化合物:Mg2ClO2-Na三、用电子式表示离子化合物的形成1
电子式:在元素符号周围用小点(或×)来表示原子的最外层电子,这种式子叫电子式
2、用电子式表示离子化合物的形成过程Mg2BrBrSKKBrMgBrS2-KK例:动画31
原子、离子都要标出最外层电子,离子须标明电荷;2
阴离子要用方括号括起来;3
相同的原子可以合并写,相同的离子要单个写;4
不能把“→”写成“====”;5
用箭头标明电子转移方向
书写要点:思考题判断下列作用属于化学键的是:(1)
水分子中,O原子与H原子之间的作用(2)
水分子中,H原子与H原子之间的作用(3)
冰中,水分子与水分子之间的作用(4)
NaCl中,钠离子与氯离子之间的作用练习题1
用电子式表示Ca、Mg2+、N3-、S2-2
用电子式表示K2O、BaCl2、Na2S3
用电子式表示MgF2、Na2S、LiCl的形成过程下列说法是否正确
1、分子内原子之间的相互作用叫化学键
2、阴、阳离子间的静电吸引作用叫做离子键
是不是所有的金属和非金属元素之间都能形成离子键
是否只有金属与非金属之间才能形成离子键