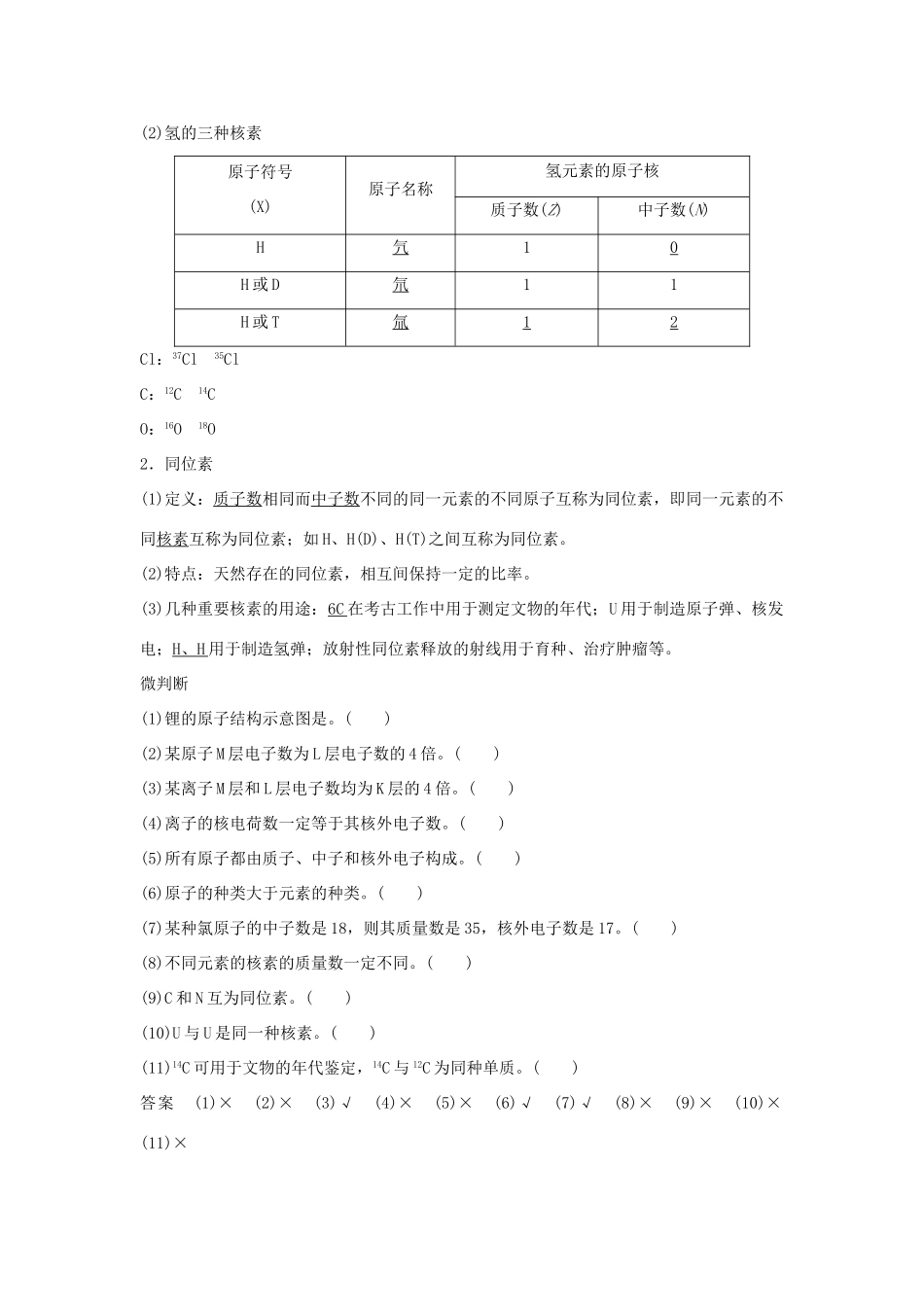
第1课时原子结构核素学业要求核心素养对接1.了解质量数的定义。2.了解原子的表示方法。3.了解原子的核外电子能量高低与分层排布的关系。4.了解核外电子分层排布的规律。5.知道元素、核素的概念。通过原子结构的学习、通过对核外电子排布规律的学习,提高学生宏观辨识与微观辨析的素养水平。[知识梳理]知识点一原子的构成、质量数如图1:原子结构的发现史,通过本图我们可以知道原子结构的认知是逐步深入的,图2表示原子结构,结合本图完成下列知识点:1.原子的构成(1)构成原子原子显电中性(2)原子的表示方法→元素符号,如Cl表示质量数为37、核电荷数为17的氯原子。阳离子:质子数>核外电子数阴离子:质子数<核外电子数2.质量数(1)质量数质子和中子的相对质量都近似为1,忽略电子的质量,将原子核内所有质子和中子的相对质量取近似整数值相加所得的数值即为质量数,用符号A表示。(2)两个关系①质量数(A)=质子数(Z)+中子数(N)(质量关系)。约为相对原子质量②原子序数=核电荷数=质子数=核外电子数(数量关系)。知识点二原子核外电子的排布如图所示,核外电子在原子核外的排布规律是用电子云来表示的,在高中阶段为了好理解出现了最后一图排布方式,结合上图,完成下列知识点:1.核外电子的分层排布在多电子的原子里,电子的能量并不相同。能量低的,通常在离核近的区域运动;能量高的,通常在离核远的区域运动。核外电子的分层运动,又叫核外电子的分层排布。其关系如下:2.原子核外电子的排布规律尝试自己写一下Na的核外电子排布知识点三核素、同位素请结合上图氢元素的不同核素结构,完成下列知识点:1.核素(1)定义:具有一定数目质子和一定数目中子的一种原子。(2)氢的三种核素原子符号(X)原子名称氢元素的原子核质子数(Z)中子数(N)H氕10H或D氘11H或T氚12Cl:37Cl35ClC:12C14CO:16O18O2.同位素(1)定义:质子数相同而中子数不同的同一元素的不同原子互称为同位素,即同一元素的不同核素互称为同位素;如H、H(D)、H(T)之间互称为同位素。(2)特点:天然存在的同位素,相互间保持一定的比率。(3)几种重要核素的用途:6C在考古工作中用于测定文物的年代;U用于制造原子弹、核发电;H、H用于制造氢弹;放射性同位素释放的射线用于育种、治疗肿瘤等。微判断(1)锂的原子结构示意图是。()(2)某原子M层电子数为L层电子数的4倍。()(3)某离子M层和L层电子数均为K层的4倍。()(4)离子的核电荷数一定等于其核外电子数。()(5)所有原子都由质子、中子和核外电子构成。()(6)原子的种类大于元素的种类。()(7)某种氯原子的中子数是18,则其质量数是35,核外电子数是17。()(8)不同元素的核素的质量数一定不同。()(9)C和N互为同位素。()(10)U与U是同一种核素。()(11)14C可用于文物的年代鉴定,14C与12C为同种单质。()答案(1)×(2)×(3)√(4)×(5)×(6)√(7)√(8)×(9)×(10)×(11)×微训练1.科学家于2000年发现了第116号元素(Lv)。下列有关质量数为293的Lv原子的描述错误的是()A.质子数为116B.中子数为177C.电子数为116D.该原子可表示为Lv答案D2.在粒子NH3D+中,电子数、质子数和中子数之比为()A.10∶7∶11B.11∶11∶8C.10∶11∶8D.11∶8∶10答案C3.下列微粒结构示意图中,不正确的是()答案B4.下列8种化学符号:H2、H2、C、Li、Na、N、Li、Mg。(1)表示核素的符号共________种。(2)互为同位素的是________和________。(3)中子数相等,但质子数不相等的核素是________和________________。解析(1)H2、H2为分子,不属于核素范畴。(2)Li、Li的质子数相同,中子数不同,二者互为同位素。(3)Na和Mg的中子数相等,但质子数不同。答案(1)6(2)LiLi(3)NaMg微思考1.1~18号元素的核外电子排布示意图是什么?提示2.一种元素可以有多种核素,决定核素的微粒是什么?如何判断不同核素是否属于同位素?提示核电荷数(质子数)决定了元素,只有确定了质子数和中子数才能确定核素;同位素属于同种元素,其质子数一定相同,故不同核素中,质子数相同的核素属于同位素。3.16O与18O互为同位素,O2与O3互为同素异形体,同位素与同素异形体有什么区别?提示(1)意义不同,同位素是指质子数相同而...