【同步知识】一
本周教学内容:高三总复习第三讲物质的量二
重点、难点:本章的主要内容是物质的量,以及摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗定律、质量分数、溶解度等一系列概念和一系列有关的计算
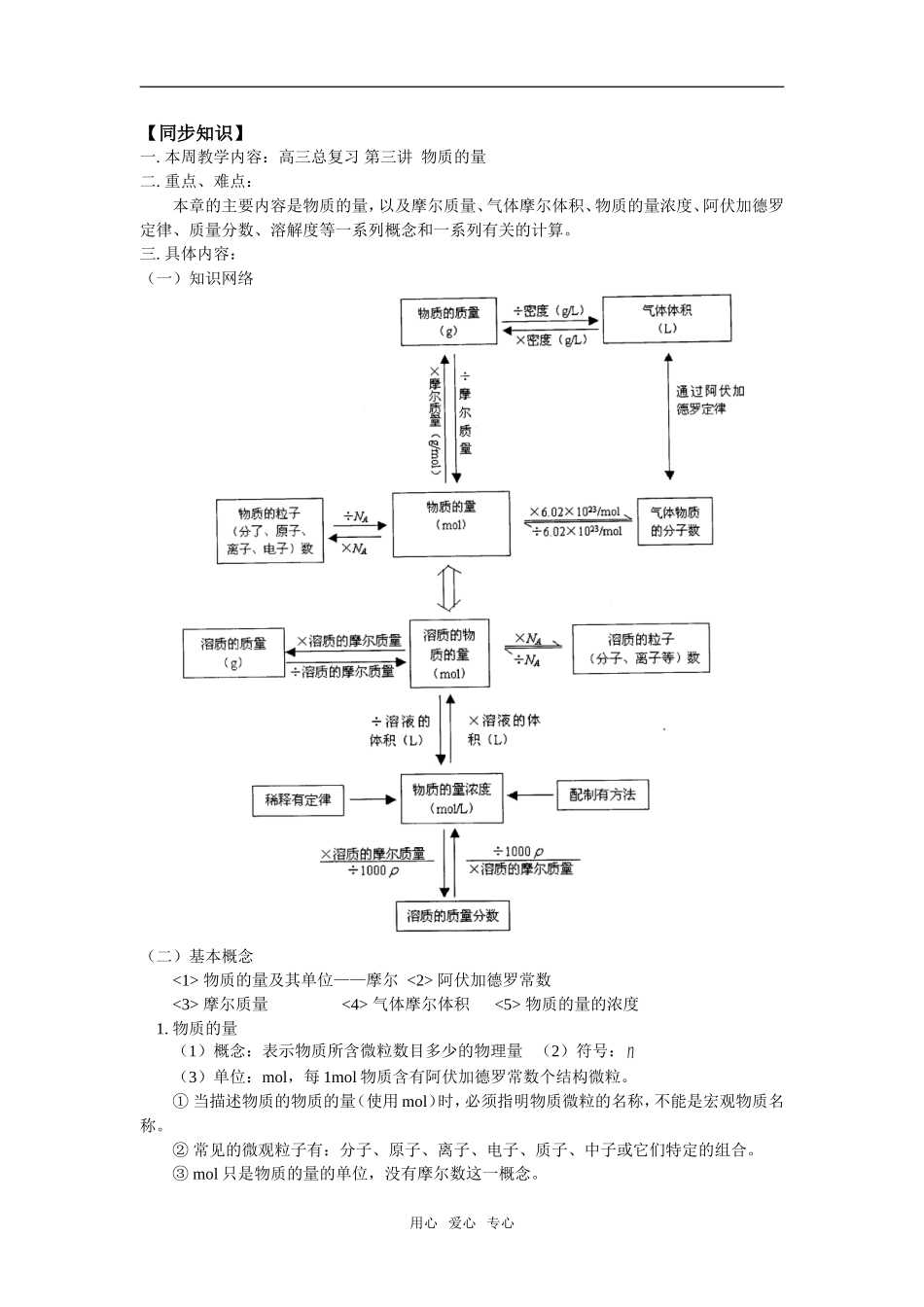
具体内容:(一)知识网络(二)基本概念物质的量及其单位——摩尔阿伏加德罗常数摩尔质量气体摩尔体积物质的量的浓度1
物质的量(1)概念:表示物质所含微粒数目多少的物理量(2)符号:(3)单位:mol,每1mol物质含有阿伏加德罗常数个结构微粒
①当描述物质的物质的量(使用mol)时,必须指明物质微粒的名称,不能是宏观物质名称
②常见的微观粒子有:分子、原子、离子、电子、质子、中子或它们特定的组合
③mol只是物质的量的单位,没有摩尔数这一概念
用心爱心专心④每mol物质含有阿伏加德罗常数个微粒
阿伏加德罗常数(1)含义:实验测定12g12C中碳原子的个数(2)符号:NA(3)单位:mol-1(4)说明:①NA的基准是12g碳-12中的原子个数②12C不仅是摩尔的基准对象,而且还是相对原子质量的基准③NA是一个实验值,现阶段常取6
02×1023作计算④要注意NA与6
02×1023的区别3
摩尔质量(1)概念:单位物质的量的物质的质量(2)符号:(3)单位:g·mol-1(4)说明:①使用范围:A
任何一种微观粒子B
无论是否纯净C
无论物质的状态②与式量的比较:③与1mol物质的质量的比较:4
气体摩尔体积(1)概念:单位物质的量的气体的体积(2)符号:(3)单位:L·mol-1(4)标准状况下的气体摩尔体积①标准状况:0℃、1atm即1
01×105Pa②理想气体:A
不计大小但计质量
不计分子间的相互作用
③标准状况下的气体摩尔体积:约22
4L·mol-1(5)影响物质体积大小的因素:①构成物质的微粒的大小(物质的本性)②结构微粒之间距离的大小(温度与压强来