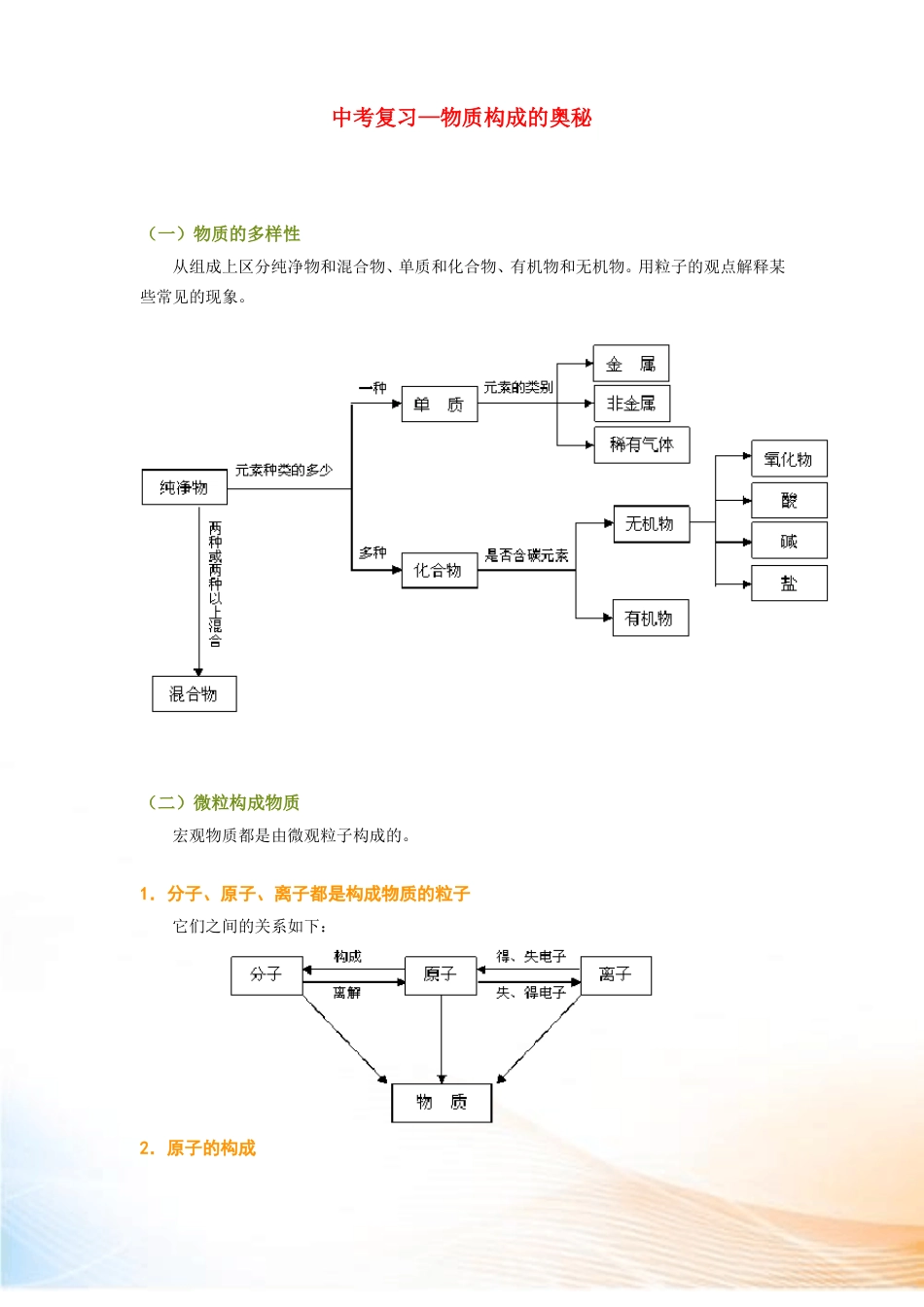
中考复习—物质构成的奥秘(一)物质的多样性从组成上区分纯净物和混合物、单质和化合物、有机物和无机物
用粒子的观点解释某些常见的现象
(二)微粒构成物质宏观物质都是由微观粒子构成的
1.分子、原子、离子都是构成物质的粒子它们之间的关系如下:2.原子的构成(1)质子数=核电荷数=原子序数=核外电子数,原子不显电性
(2)质子数+中子数=相对原子质量(数值),原子的质量主要集中在原子核上
(3)不是所有原子的原子核都有中子
(4)核外电子是分层排布的(认识原子结构示意图)
3.分子和原子的本质区别(1)分子的定义:分子是保持物质化学性质的最小粒子
提示:分子在物理变化中不可分,分子间的距离可变化;分子在化学变化中可分,构成分子的原子可重新组合,构成新的分子
原子的定义:原子是化学变化中的最小粒子
提示:原子在化学变化中不可分,但原子可重新组合
(2)认识分子的主要性质,并能用分子的性质解释一些基本问题
a.分子的体积和质量都很小b.分子总是在不停地运动c.分子间有一定的间隔d.分子在化学变化中可分(三)化学元素1.定义:元素是具有相同核电荷数(即核内质子数)的一类原子的总称
已经发现的元素有一百余种
地壳里和生命细胞中含量最多的元素是氧
地壳里含量较多的元素还有:硅、铝、铁、钙、钠、钾、镁等;生命细胞中含量较多的元素还有:碳、氢、氮、钙、磷等
2.两个决定:在原子结构中,核内质子数决定元素的种类;最外层电子数主要决定元素的化学性质
3.元素的简单分类:金属元素、非金属元素和稀有气体元素
元素的简单分类金属元素非金属元素稀有气体元素4.一些常见元素的名称和符号5.提示:元素只论种类,不论个数
最外层电子数一般为1~3个一般为5~7个8个(氦为2个)化学性质较易失电子形成阳离子较易得电子形成阴离子化学性质稳定(四)物质组成的表示1.物质的构成2.物质组成的表示3.化学式:表示物质的组