练8化学反应的能量变化及热化学方程式(A组)1.下列与化学反应能量变化相关的叙述正确的是()A
生成物总能量一定低于反应物总能量B
放热反应的反应速率总是大于吸热反应的反应速率C
应用盖斯定律,可计算某些难以直接测量的反应焓变D
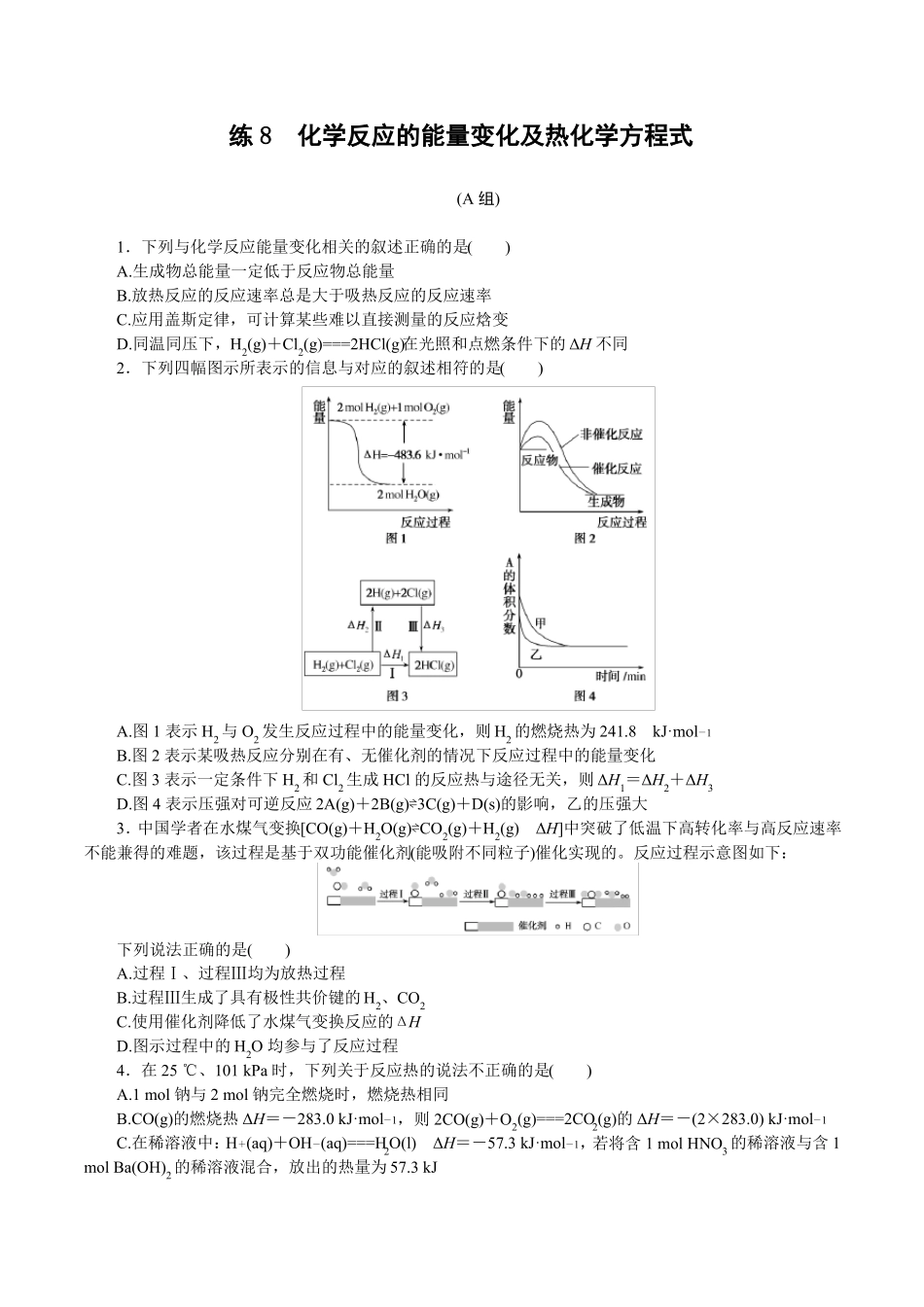
同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同2.下列四幅图示所表示的信息与对应的叙述相符的是()A
图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241
8kJ·mol1B
图2表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化C
图3表示一定条件下H2和Cl2生成HCl的反应热与途径无关,则ΔH1=ΔH2+ΔH3D
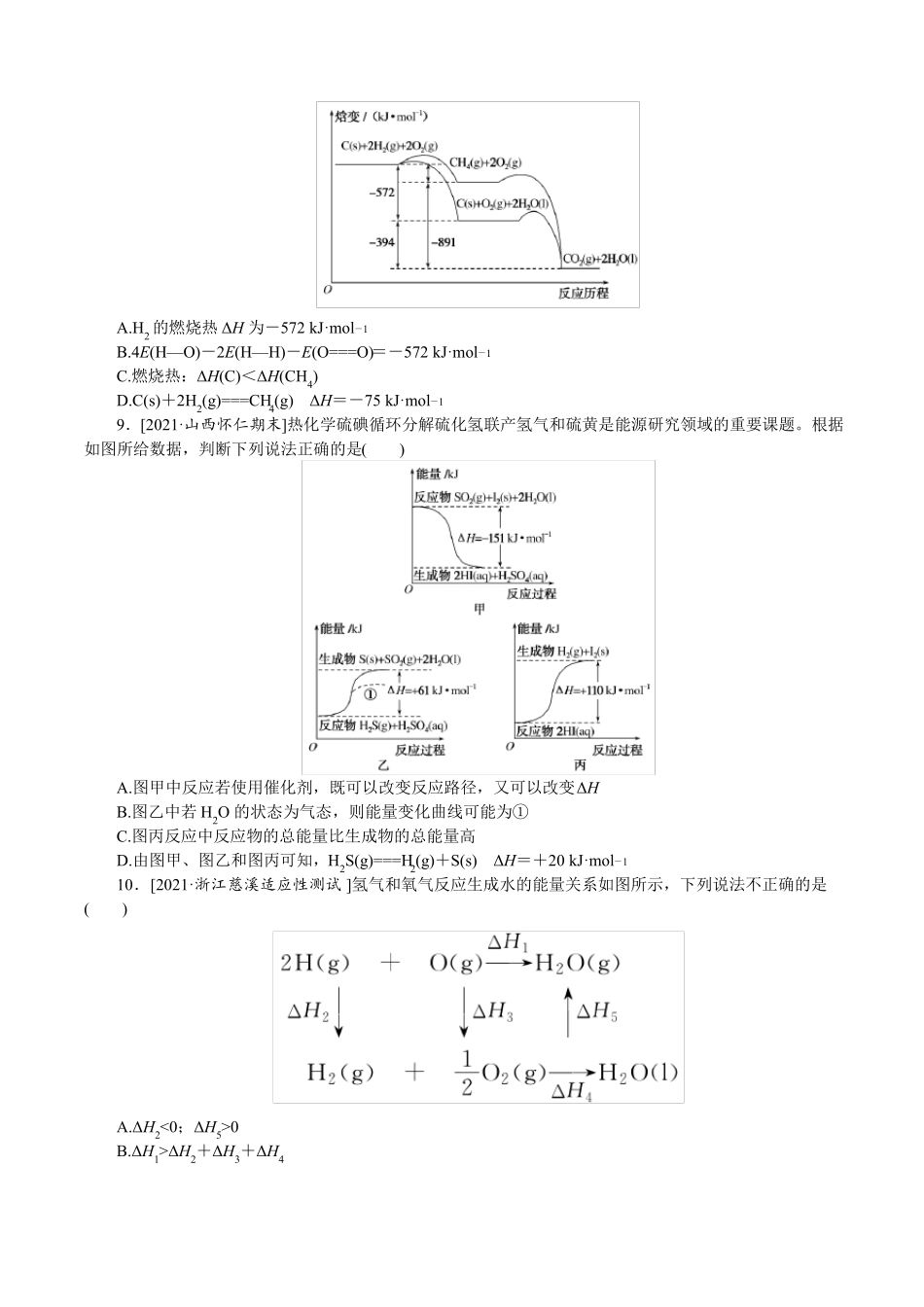
图4表示压强对可逆反应2A(g)+2B(g)⇌3C(g)+D(s)的影响,乙的压强大3.中国学者在水煤气变换[CO(g)+H2O(g)⇌CO2(g)+H2(g)ΔH]中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的
反应过程示意图如下:-下列说法正确的是()A
过程Ⅰ、过程Ⅲ均为放热过程B
过程Ⅲ生成了具有极性共价键的H2、CO2C
使用催化剂降低了水煤气变换反应的ΔHD
图示过程中的H2O均参与了反应过程4.在25℃、101kPa时,下列关于反应热的说法不正确的是()A
1mol钠与2mol钠完全燃烧时,燃烧热相同--B
CO(g)的燃烧热ΔH=-283
0kJ·mol1,则2CO(g)+O2(g)===2CO2(g)的ΔH=-(2×283
0)kJ·mol1+--C
在稀溶液中:H(aq)+OH(aq)===H2O(l)ΔH=-57
3kJ·mol1,若将含1molHNO3的稀溶液与含1molBa(OH)2的稀溶液混合,放出的热量为57
2gH2完全燃烧生成液态水,放出285
8kJ热量,氢气燃烧的热化学