2022年高考化学热点《循环催化机理、多重平衡体系、图表数据处理》第一部分:催化剂1、(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯晴(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:①C3H6(g)+NH3(g)+3/2O2(g)=C3H3N(g)+3H2O(g)ΔH=−515kJ·mol−1−1②C3H6(g)+O2(g)=C3H4O(g)+H2O(g)ΔH=−353kJ·mol提高丙烯腈反应选择性的关键因素是
....2、丙烯是一种重要的有机化工原料,用于制丙烯腈、环氧丙烷、丙酮等
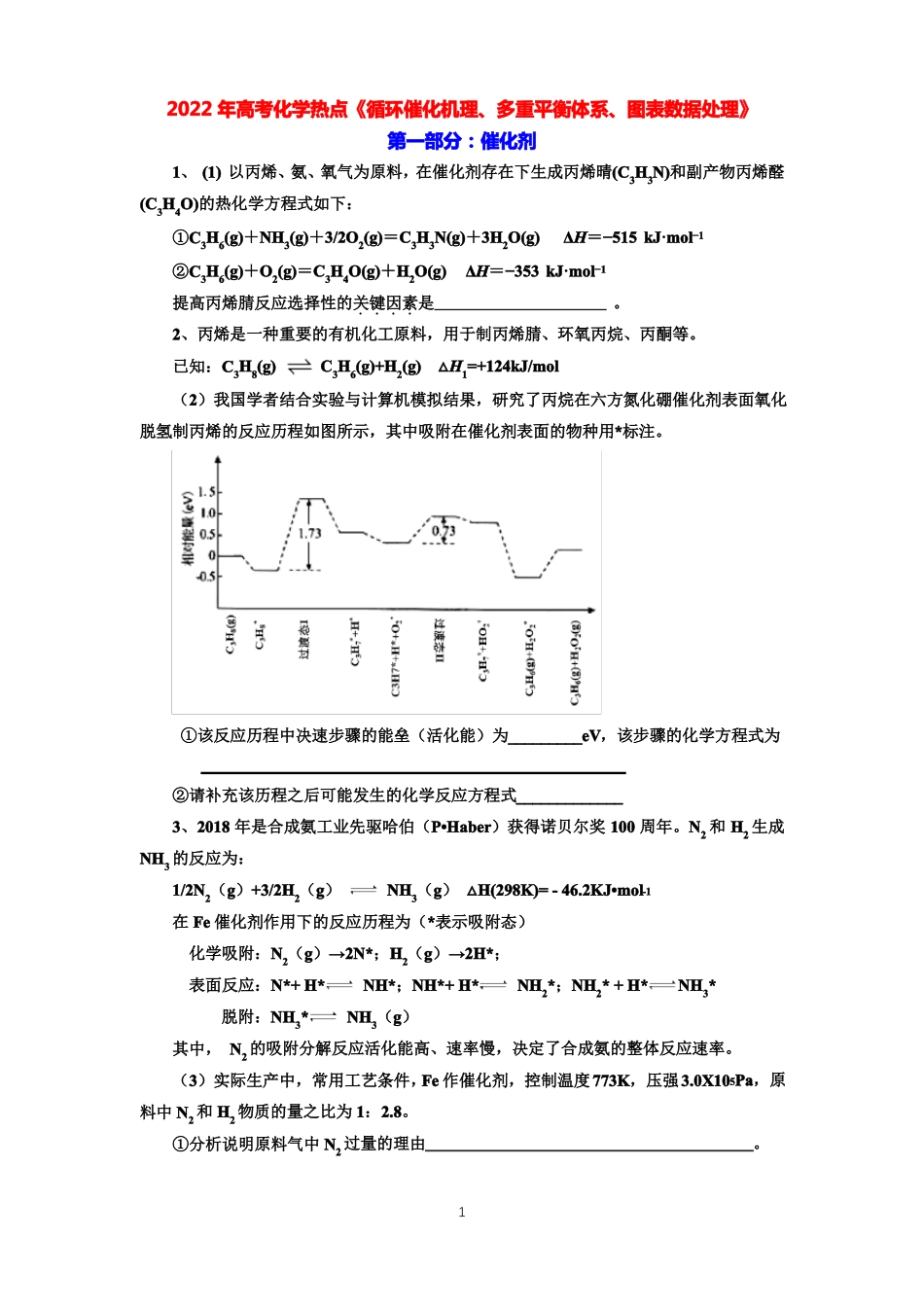
已知:C3H8(g)C3H6(g)+H2(g)△H1=+124kJ/mol(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程如图所示,其中吸附在催化剂表面的物种用*标注
①该反应历程中决速步骤的能垒(活化能)为_________eV,该步骤的化学方程式为②请补充该历程之后可能发生的化学反应方程式_____________3、2018年是合成氨工业先驱哈伯(P•Haber)获得诺贝尔奖100周年
N2和H2生成NH3的反应为:1/2N2(g)+3/2H2(g)NH3(g)△H(298K)=-46
2KJ•mol-1在Fe催化剂作用下的反应历程为(*表示吸附态)化学吸附:N2(g)→2N*;H2(g)→2H*;表面反应:N*+H*脱附:NH3*NH*;NH*+H*NH3(g)NH2*;NH2*+H*NH3*其中,N2的吸附分解反应活化能高、速率慢,决定了合成氨的整体反应速率
(3)实际生产中,常用工艺条件,Fe作催化剂,控制温度773K,压强3
0X105Pa,原料中N2和H2物质的量之比为1:2
①分析说明原料气中N2过量的理由
14、(2021年山东省济南模拟-19)采用镍系催化剂的水煤气(主要有效成分为CO和H2)甲烷化