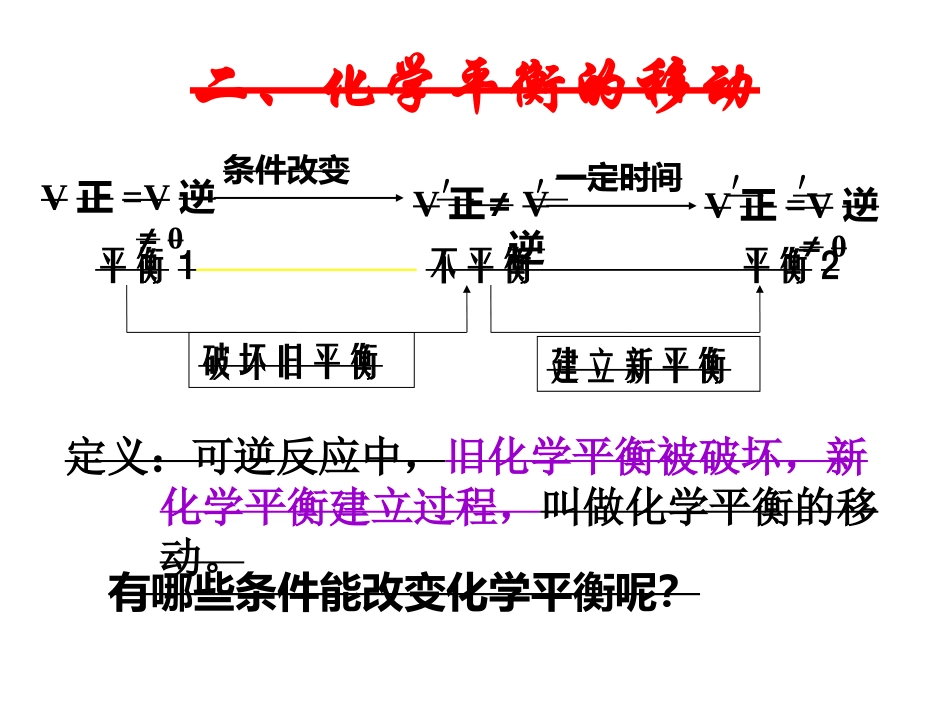
定义:可逆反应中,旧化学平衡被破坏,新化学平衡建立过程,叫做化学平衡的移动
V正≠V逆V正=V逆≠0条件改变平衡1不平衡平衡2建立新平衡破坏旧平衡V正=V逆≠0′′一定时间二、化学平衡的移动′′有哪些条件能改变化学平衡呢
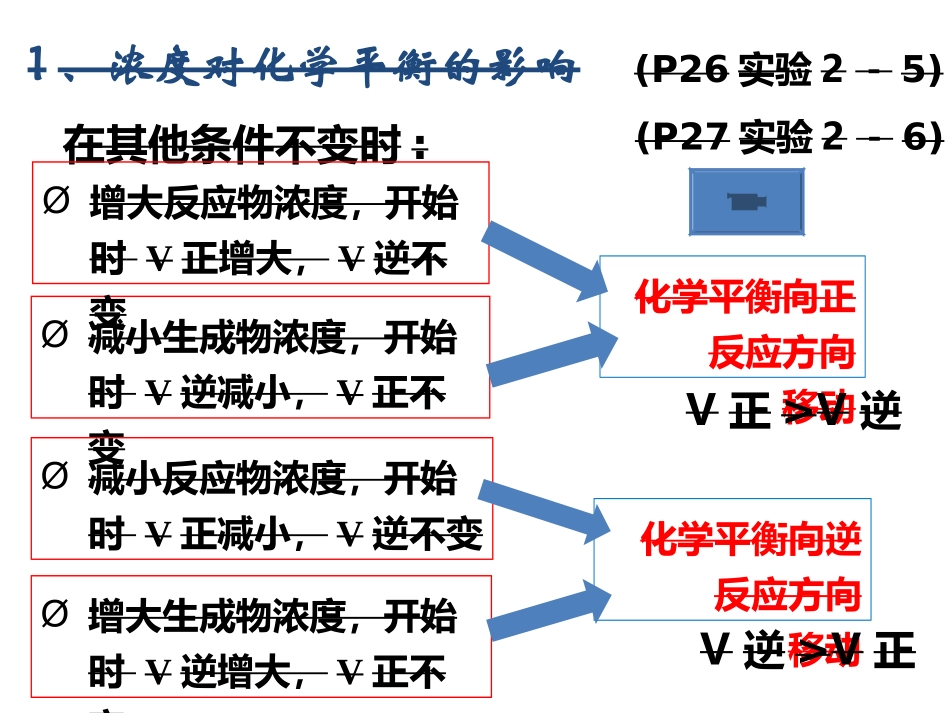
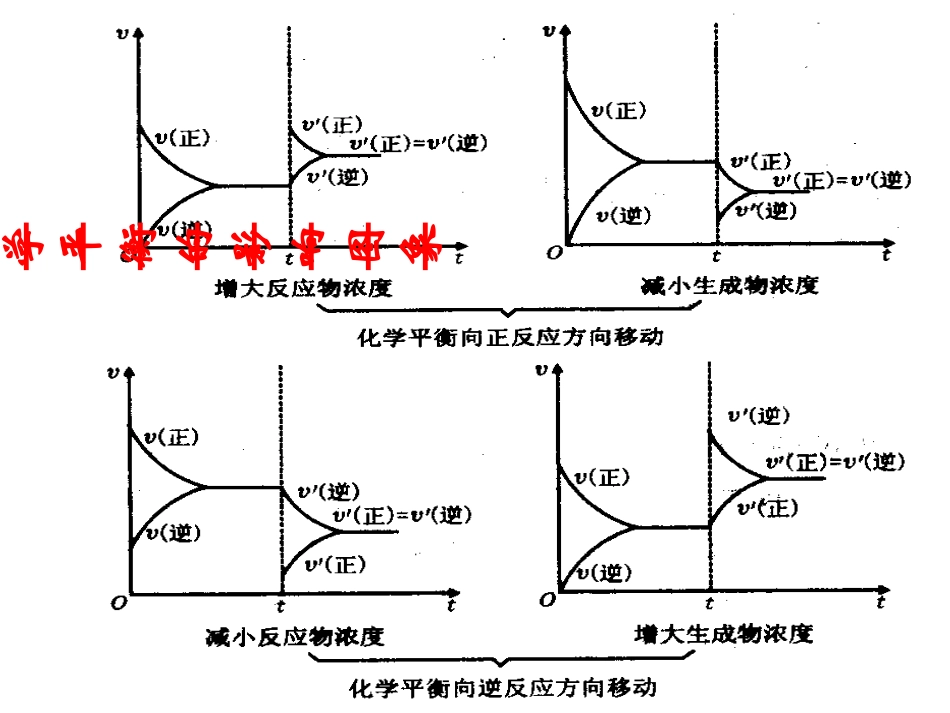
1、浓度对化学平衡的影响化学平衡向逆反应方向移动在其他条件不变时:Ø减小生成物浓度,开始时V逆减小,V正不变Ø增大反应物浓度,开始时V正增大,V逆不变化学平衡向正反应方向移动Ø减小反应物浓度,开始时V正减小,V逆不变Ø增大生成物浓度,开始时V逆增大,V正不变(P26实验2-5)(P27实验2-6)V正>V逆V逆>V正浓度对化学平衡的影响图象Ø浓度对化学平衡移动的几个注意点①对平衡体系中的固态和纯液态物质,其浓度可看作一个常数,增加或减小固态或液态纯净物的量并不影响V正、V逆的大小,所以化学平衡不移动
②只要是增大浓度,不论增大的是反应物浓度,还是生成物浓度,新平衡状态下的反应速率一定大于原平衡状态;减小浓度,新平衡状态下的速率一定小于原平衡状态
③反应物有两种或两种以上,增加一种物质的浓度,该物质的平衡转化率降低,而其他物质的转化率提高
④改变浓度后,速率-时间图象是连续的
在工业生产中适当增大廉价的反应物的浓度,使化学平衡向正反应方向移动,可以提高价格较高原料的转化率,以降低生产成本2SO2(g)+O2(g)SO3(g)的平衡体系中,为了提高SO2的利用率,可采用什么措施
可逆反应H2O(g)+C(s)CO(g)+H2(g)在一定条件下达到平衡状态,改变下列条件,能否引起平衡移动
CO的浓度有何变化
①增大水蒸气浓度②加入更多的碳③增加H2浓度①平衡正向移动,CO浓度增大②平衡不移动,CO浓度不变③平衡逆向移动,CO浓度减小2、温度对化学平衡的影响在其它条件不变的情况下:Ø温度升高,V正、V逆都增大,平衡向着吸热反应的方向移动Ø温度降低