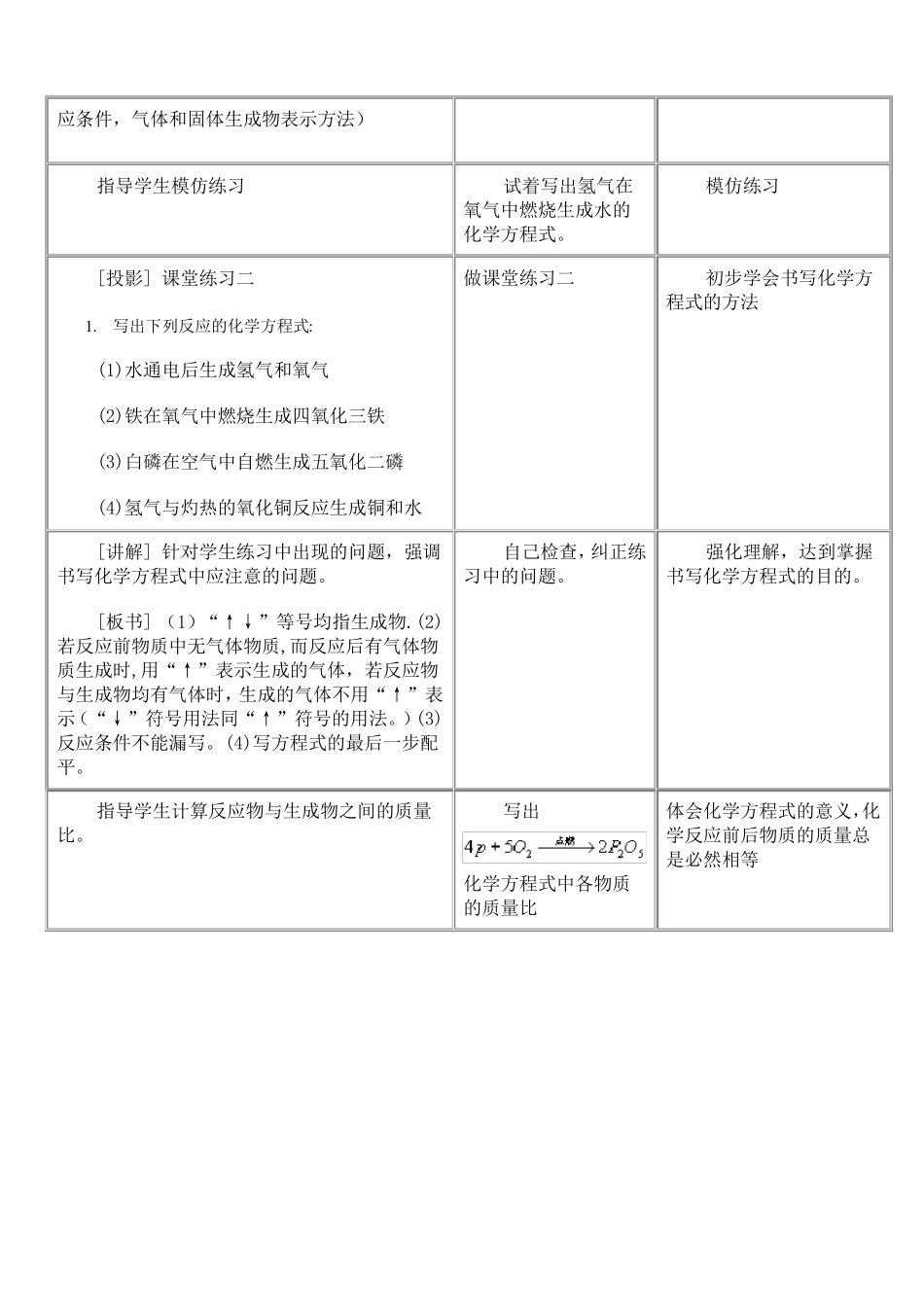
化学方程式一.教学目的1
学会从用化学式表示某种物质到学会用化学式来表示化学反应
通过对具体化学反应的分析,理解化学方程式的意义及书写化学方程式应遵循的原则
初步学会书写化学方程式的方法,掌握书写要领
二.教学重点1
正确书写化学方程式,包括反应物、生成物的正确的表示方法,反应条件的表示,配平化学反应方程式
根据文字描述反应正确写出化学反应方程式
三.教学难点1
化学方程式的配平
根据文字描述正确写出化学反应方程式并配平
四.教学方法问题探讨法
五.教学过程教师活动[问题引入]我们学习了质量守恒定律,那么,在化学上的有没有一种式子,既能表示反应物和生成物是什么,又能反映出该化学变化遵循质量守恒定律呢
回答是肯定的,这就是我们本节课要学习的一种化学用语——化学方程式
[板书]一、化学方程式1.定义:用化学式来表示化学反应的方程式,叫做化学方程式
将碳+氧气二氧化碳的文字表达式改写成用化学式来表示的化学方程式
初步认识化学方程式学生活动引起思考,产生学生欲望和兴趣
同时还回忆上节课学习的内容,温故知新
教学意图问题导思激发兴趣[问题讨论]同学们,听到”方程式”是不是会让同学们想起数学课中学过的方程式,等式左右两边是相等的,那么化学方程式是否也是如此
它表示了什么
它与文字表达式有什么不同
指导学生看书49页的读图
[板书]二、化学方程式的意义:1
表示参加反应的物质,生成的物质2
各物质间原子和分子个数比
表示反应条件
表示反应物和生成物的质量比
课堂练习一(投影)试写出下列反应的化学方程式:1
硫在氧气中燃烧生成二氧化硫2
磷在氧气中燃烧生成五氧化二磷让学生在练习中发现问题看书,讨论化学方程式的意义
培养阅读能力和思维能力领会化学方程式在质和量两方面的意义
领会学习的意义完成课堂练习一创设问题情境[问题讨论]现在同学们已经完成了这个练习,同学们互相之间