【创新设计】(江苏专用)高考化学二轮题型专攻微题型13化学反应速率与化学平衡原理的综合应用(含新题,含解析)[题型专练]1.为了探究温度、硫酸铜对锌与稀硫酸反应速率的影响规律,某同学设计如下方案:编号纯锌粉质量0
2mol·L-1硫酸体积温度硫酸铜固体质量Ⅰ2
0mL25℃0Ⅱ2
0mLt℃0Ⅲ2
0mL35℃0
0mL35℃4
0g下列推断合理的是()A.为了选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,必须控制t=25B.待测物理量是收集等体积(相同条件)气体所需要的时间,时间越长,反应越快C.根据该方案,还可以探究硫酸浓度对反应速率的影响D.根据该实验方案得出反应速率大小可能是Ⅲ>Ⅱ>Ⅰ>Ⅳ解析A项,根据控制变量法,若选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,温度必须控制在35℃,错误,B项,收集相同条件下等体积的气体所需时间越长,则反应速率越慢,错误;C项,三个实验中硫酸的浓度均相同,故无法探究硫酸浓度对反应速率的影响,错误;D项,本题影响反应速率大小的主要因素是温度和硫酸铜固体的质量,由A项分析可知实验Ⅱ温度应为35℃,则反应速率Ⅱ>Ⅰ,实验Ⅲ,锌与置换出的铜构成原电池
反应速率比Ⅱ快,实验Ⅳ中由于CuSO4过多,置换出的铜可能覆盖在锌表面而阻止反应的进行,使反应速率大大减小,故四个反应的反应速率大小关系可能为Ⅲ>Ⅱ>Ⅰ>Ⅳ
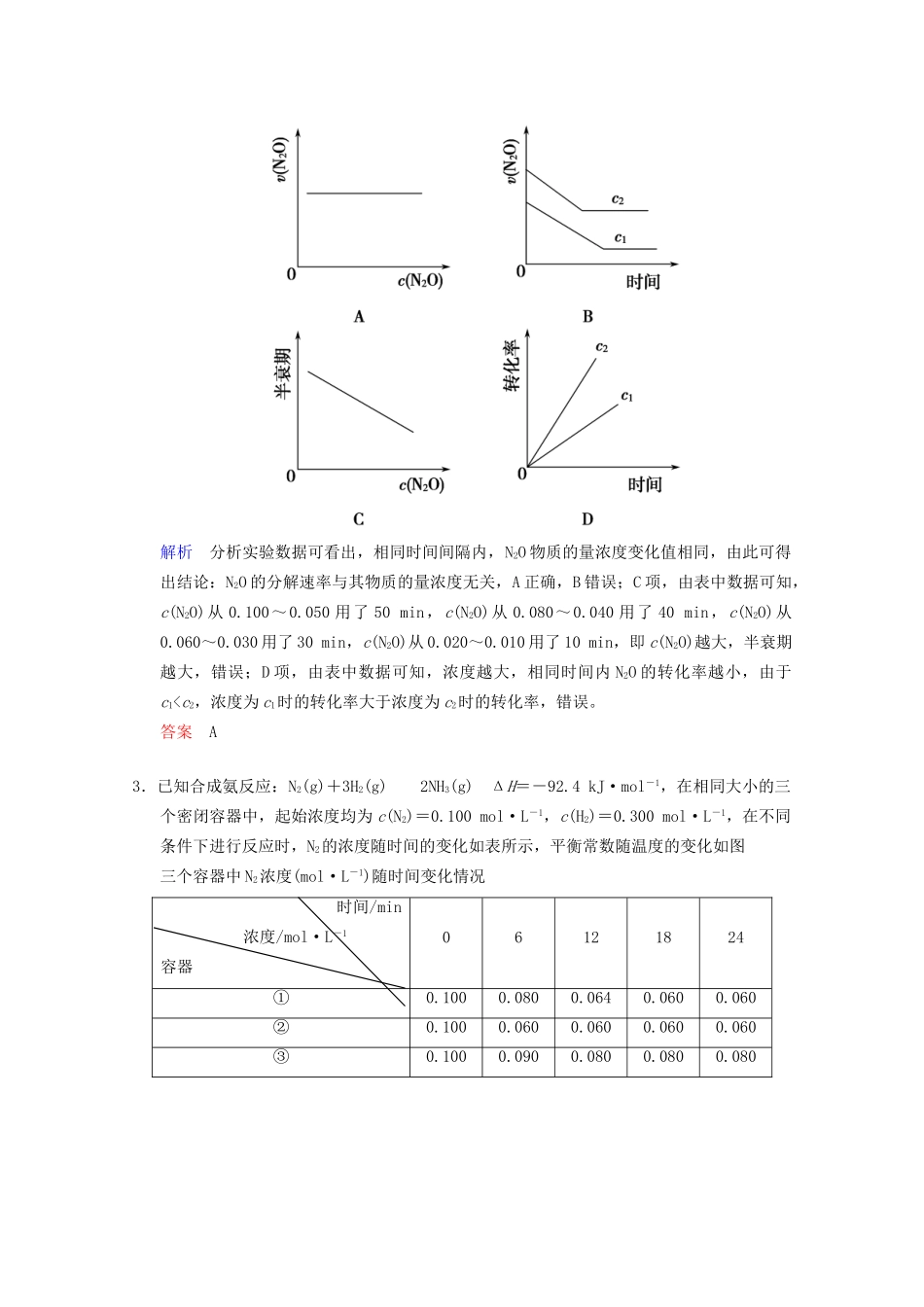
答案D2.在一定条件下,N2O分解的部分实验数据如下:反应时间/min0102030405060708090100c(N2O)/(mol·L-1)0
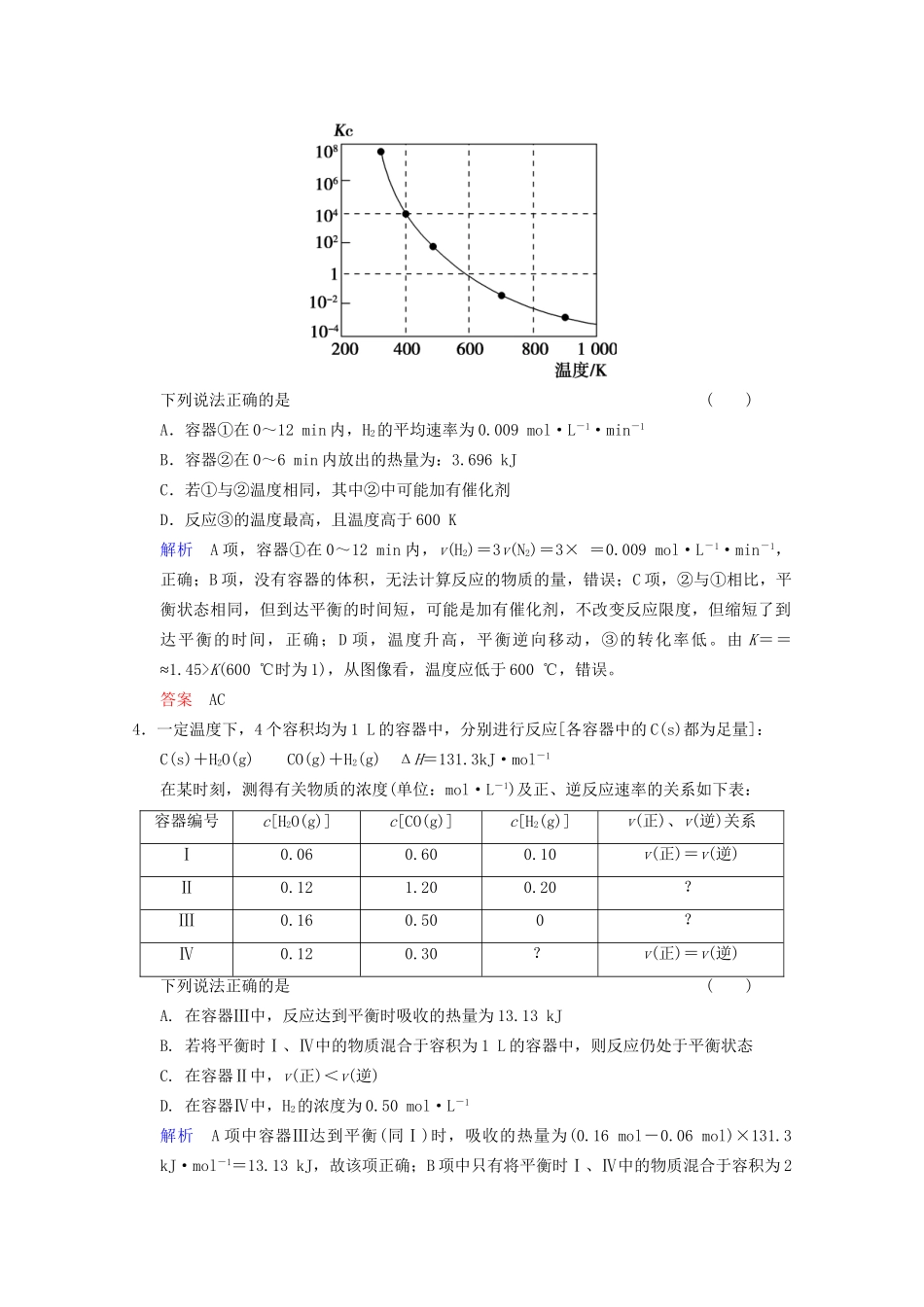
000下图能正确表示该反应有关物理量变化规律的是()(注:图中半衰期指任一浓度N2O消耗一半时所需的相应时间,c1、c2均表示N2O初始浓度且c1