“控制变量法”探究影响反应速率的因素1.(2018·哈尔滨调研)为了探究温度、不活泼金属杂质对锌与稀硫酸反应速率的影响,设计如下实验方案:编号m(Zn)/g0
1mol·L-1V(H2SO4)/mL温度/℃m(CuSO4)/gⅠ1
0250Ⅱ1
0402下列推断合理的是()A.根据该实验方案得出反应速率大小可能是Ⅲ>Ⅳ>Ⅱ>ⅠB.选择实验Ⅱ和Ⅲ探究硫酸铜对反应速率的影响,必须控制t=25C.根据该方案,可以探究温度、不活泼金属及用量对锌和稀硫酸反应速率的影响D.待测物理量是收集等体积气体所需要的时间,时间越长,反应速率越大2.(2019·马鞍山模拟)某探究小组利用丙酮的溴代反应(CH3COCH3+Br2―→CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系
反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定
在一定温度下,获得如下实验数据:实验序号初始浓度c/mol·L-1溴颜色消失所需时间t/sCH3COCH3HClBr2①0
0010290②1
0010145③0
0010145④0
0020580分析实验数据所得出的结论不正确的是()A.增大c(CH3COCH3),v(Br2)增大B.实验②和③的v(Br2)相等C.增大c(HCl),v(Br2)增大D.增大c(Br2),v(Br2)增大3.以反应5H2C2O4+2MnO+6H+===10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”
实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢
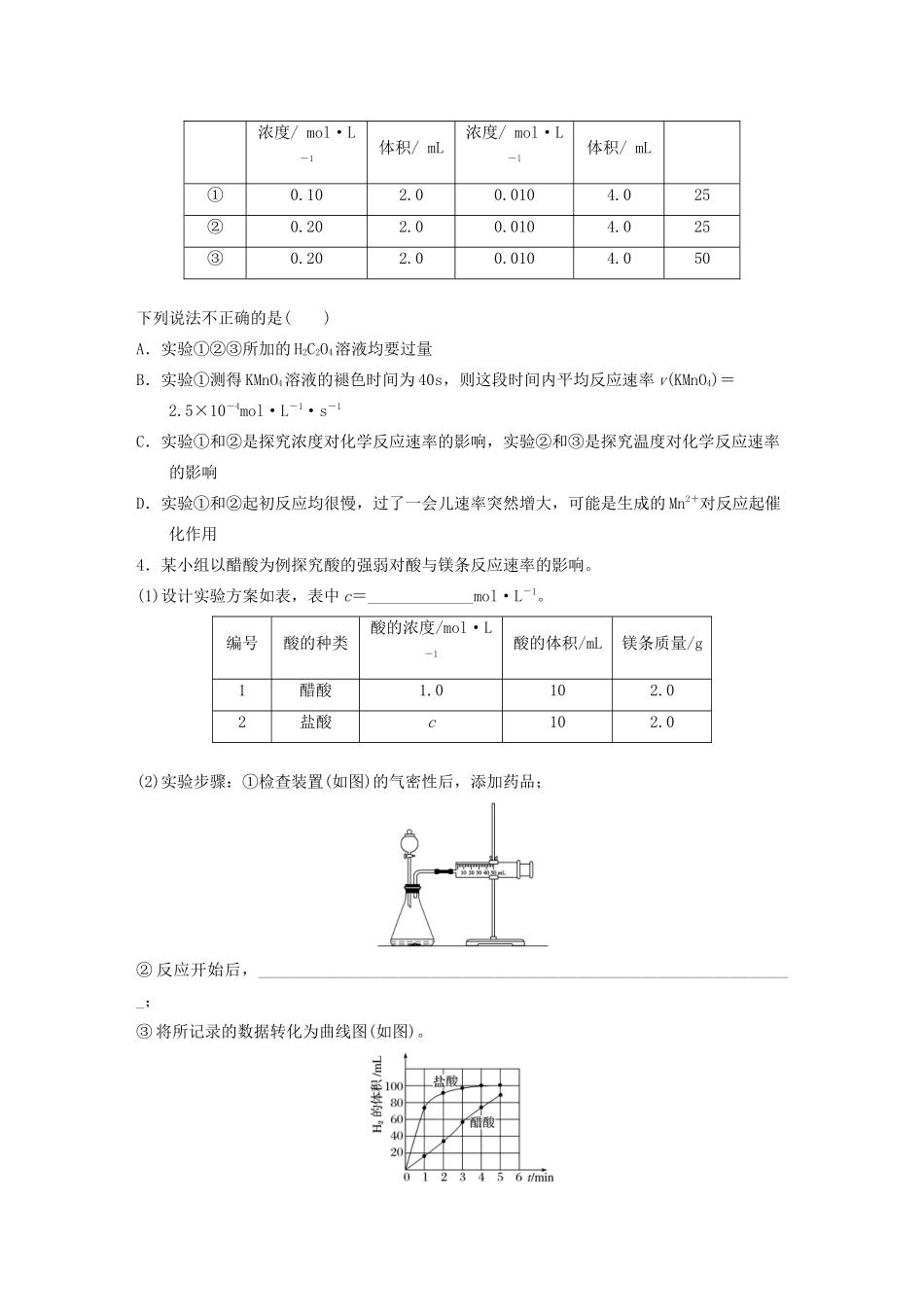
编号H2C2O4溶液酸性KMnO4溶液温度/℃浓度/mol·L-1体积/mL浓度/mol·L-l体积/mL