离子化学式与化合价【复习目标】1.初步了解核外电子是分层运动——分层排布的
2.了解离子形成的过程,认识离子也是构成物质的一种粒子
理解化学式的概念及含义
知道并初步学会应用常见元素、原子团的化合价
初步掌握化学式计算物质的相对分子质量和化合物中各元素质量比以及化合物中某元素的质量分数
知识回顾:1.核外电子的排布
(1)核外电子的分层排布:元素的原子核外的电子层最少有1层,最多有7层;第一层不超过个电子,第二层不超过个电子,最外层不超过个电子(只有1个电子层的最外层不超过2个电子)
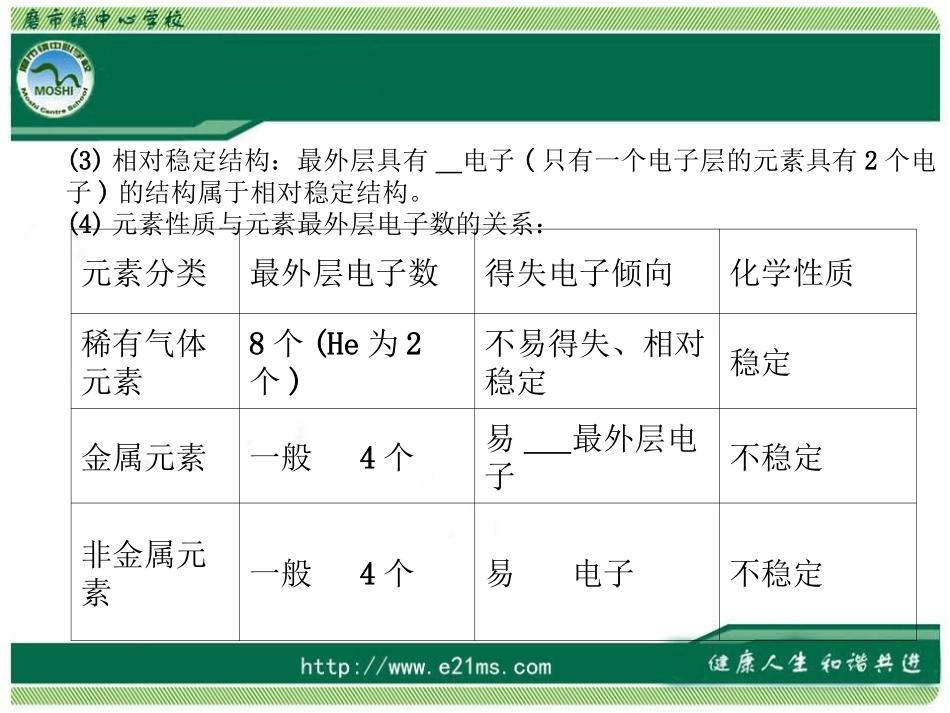
(2)原子结构简图各部分的意义:(3)相对稳定结构:最外层具有电子(只有一个电子层的元素具有2个电子)的结构属于相对稳定结构
(4)元素性质与元素最外层电子数的关系:元素分类最外层电子数得失电子倾向化学性质稀有气体元素8个(He为2个)不易得失、相对稳定稳定金属元素一般4个易最外层电子不稳定非金属元素一般4个易电子不稳定(5)元素的性质,特别是元素的化学性质,是由决定的
2.离子的形成
(1)离子:因得失电子而带电荷的原子叫离子
如Na+、Cl-、OH-、SO42-等(2)离子的分类
阳离子:带正电的离子离子阴离子:带负电的离子写法:在元素符号的右上角标明电量和电性(电量为1的省略不写)如:Na+、Mg2+、Al3+;Cl-、S2-、O2-……碳酸根离子:,氢离子:,2个亚铁离子:,5个钙离子:下列符号表示的意义:NO3-:,7Fe3+,2H+(3)离子符号及其意义(数字“2”的意义)
例如,指出下列符号中数字的意义:Fe2+,nCO2,3Cl-,5SO42-,3.离子与原子的区别和联系:阳离子原子粒子种类原子离子阳离子阴离子区别粒子结构质子数=核外电子数质子数>核外电子数质子数