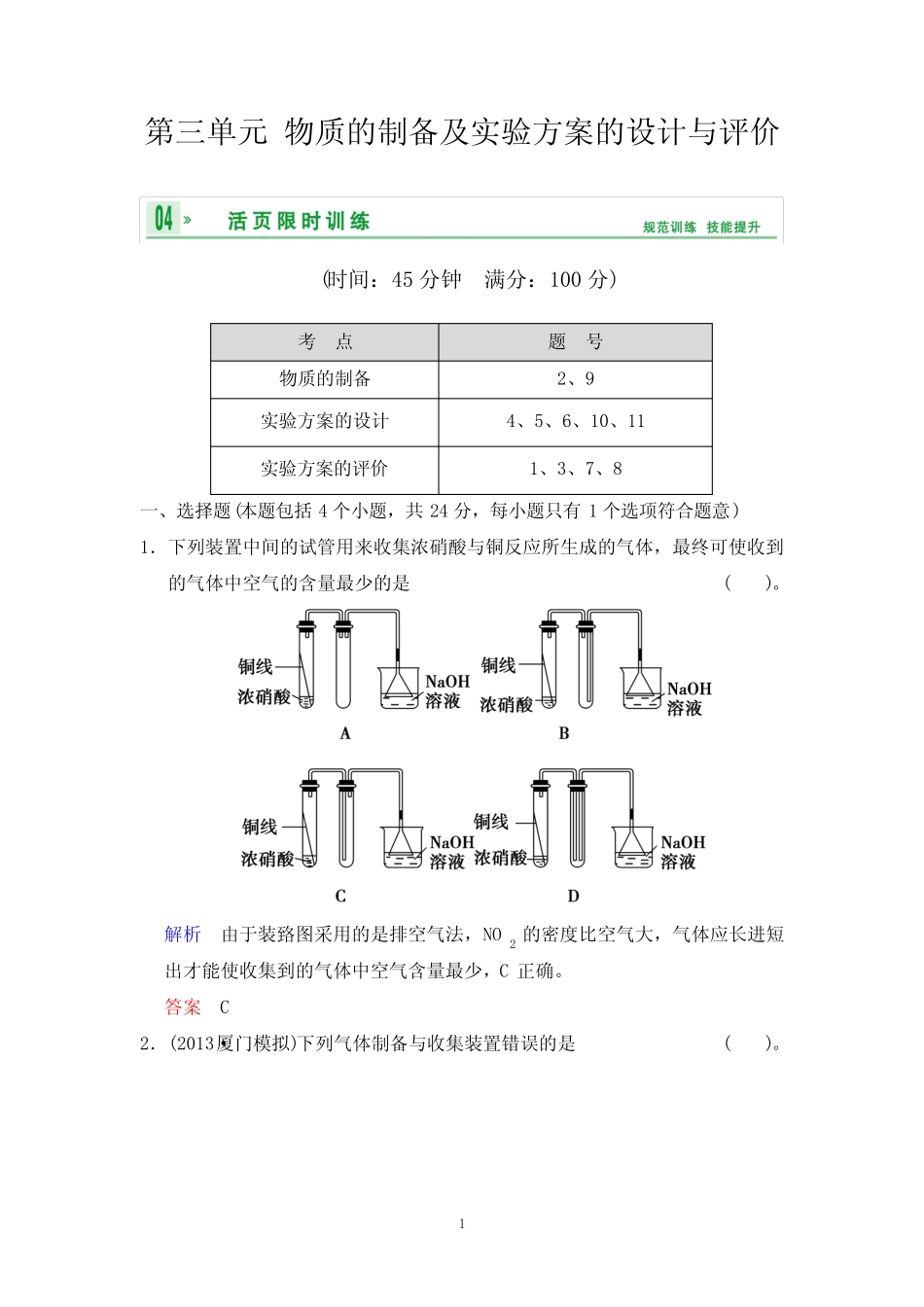
1第三单元物质的制备及实验方案的设计与评价(时间:45分钟满分:100分)考点题号物质的制备2、9实验方案的设计4、5、6、10、11实验方案的评价1、3、7、8一、选择题(本题包括4个小题,共24分,每小题只有1个选项符合题意)1.下列装置中间的试管用来收集浓硝酸与铜反应所生成的气体,最终可使收到的气体中空气的含量最少的是()。解析由于装臵图采用的是排空气法,NO2的密度比空气大,气体应长进短出才能使收集到的气体中空气含量最少,C正确。答案C2.(2013·厦门模拟)下列气体制备与收集装置错误的是()。2解析D选项,NO气体易与空气中氧气发生反应,且其密度与空气非常相近,不能用排空气法收集。答案D3.(2013·镇江中学一模)在实验室进行物质制备,下列设计的实验方案中,理论上正确、操作上可行、经济上合理的是()。A.C―――――――→在空气中点燃CO――――→CuO,△CO2―――――――→NaOH溶液Na2CO3B.Cu―――――――――→AgNO3溶液Cu(NO3)2溶液――――――→NaOH溶液Cu(OH)2C.Fe――――→点燃Fe2O3―――――――→H2SO4溶液Fe2(SO4)3溶液D.CaO――――→H2OCa(OH)2溶液――――――→Na2CO3溶液NaOH溶液解析A中的碳在空气中燃烧,无法控制只产生CO,而且操作麻烦,况且NaOH的价格比Na2CO3要贵,所以A的方案从原则来看是不符合要求的;B中AgNO3价格昂贵用来制取Cu(OH)2经济上不合算;C中铁燃烧的产物是Fe3O4,D中由生石灰制备价格较高的NaOH,中间利用了水和Na2CO3,所以这个方案设计符合题目要求。答案D4.为测定碳酸钠的质量分数(设含杂质碳酸氢钠),某学生设计了如下实验方案,下列对实验方案的叙述正确的是()。3A.称量所需要的仪器是托盘天平B.样品放在蒸发皿中灼烧C.样品中碳酸钠的质量分数为0.76D.如果灼烧后的样品放在空气中冷却,会造成实验结果偏大解析托盘天平不可能精确到小数点后三位;灼烧应放在坩埚中,而不是蒸发皿中;碳酸氢钠受热分解生成碳酸钠,根据化学反应方程式计算,求出碳酸钠的质量分数为0.892;灼烧后的样品放在空气中冷却,碳酸钠吸水,会造成实验结果偏大。答案D二、选择题(本题包括3个小题,共18分,每小题有1~2个选项符合题意)5.(2013·苏北四市一调)下列实验操作、现象与结论对应关系正确的是()。选项实验操作实验现象结论A向某溶液中先滴加盐酸无现象,再滴加BaCl2溶液有白色沉淀生成原溶液中含有SO42-B向AgCl沉淀中滴入稀KI溶液白色沉淀变黄AgI比AgCl更难溶C向无水乙醇中加入浓H2SO4,加热至170℃,将产生的气体通入酸性KMnO4溶液紫红色褪去使溶液褪色的气体一定是乙烯D向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热无砖红色沉淀生成淀粉没有水解生成葡萄糖解析用乙醇与浓硫酸加热制乙烯的实验中,要检验产物是否是乙烯时要注意产物中可能混有乙醇和SO2,它们均能使酸性KMnO4溶液褪色,C项错误;用新制的Cu(OH)2悬浊液检验淀粉水解产物中是否有葡萄糖时,必须先用NaOH溶液中和H2SO4,否则Cu(OH)2悬浊液会与H2SO4反应而干扰葡萄糖4的检验,D项错误。答案AB6.(2011·广东高考)某同学通过系列实验探讨Mg及其化合物的性质,操作正确且能达到目的的是()。A.将水加入浓硫酸中得稀硫酸,置镁片于其中探讨Mg的活泼性B.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀D.将Mg(OH)2沉淀转入表面皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体解析浓硫酸稀释时,应将浓硫酸沿玻璃棒缓慢加入水中并用玻璃棒不断搅拌以防止液滴飞溅,A项错误;将NaOH溶液与MgSO4溶液混合即可得到Mg(OH)2沉淀,B项正确;过滤时,应使用玻璃棒引流,C项错误;对MgCl2溶液直接加热,Mg2+易水解,不能得到MgCl2固体,D项错误。答案B7.(2013·扬州质检)下列实验操作、现象与实验结论一致的是()。选项实验操作、现象实验结论A将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别滴加CCl4,振荡,静置氧化性:Fe3+>Br2>I2B除锈的铁钉在浓硝酸中浸泡后,用蒸馏水洗净,再放入CuSO4溶液中无现象铁钉表面形成了一层致密稳定的氧化膜C向某溶液中加入Ba(NO3)2...