1分子的定义原子的定义2构成物质的微粒有分子、原子、离子,其中由原子直接构成的物质(金属、稀有气体)3分子原子的本质区别:4分子由-----构成5分子的特征6用分子的观点解释物理变化:分子不变化学变化:分子改变纯净物:同种分子(分子相同)混合物:多种分子(分子不同)7水的化学性质由——保持,氧气的化学性质由——保持,8物质在不同条件下的三态变化主要是
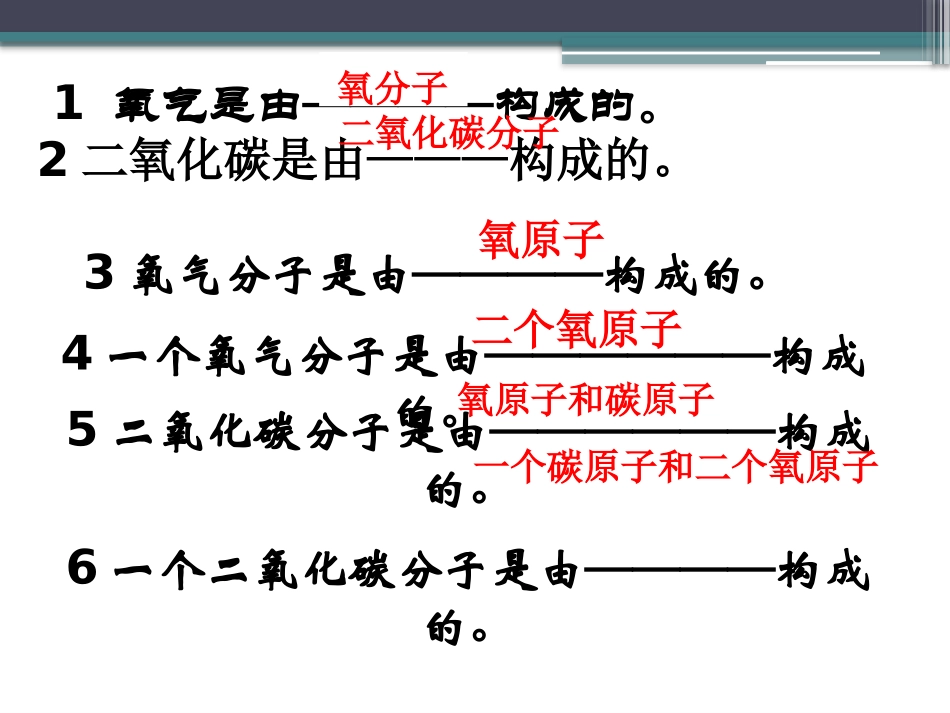
水变成水蒸气,其原因是—————————复习回顾氧分子水分子分子的间隔发生变化水分子的间隔改大了在化学变化中,分子可分,原子不可分原子3氧气分子是由————构成的
4一个氧气分子是由——————构成的
5二氧化碳分子是由——————构成的
6一个二氧化碳分子是由————构成的
1氧气是由————构成的
2二氧化碳是由———构成的
二氧化碳分子氧分子氧原子二个氧原子氧原子和碳原子一个碳原子和二个氧原子在化学变化中,分子可以分成原子,而原子不能再分
那么,原子是不是简单而不可分割的实心球体呢
学习目标1、认识质子、中子、电子是如何构成原子的2、了解质子、中子、电子的质量以及电性3、知道相对原子质量的意义1803年英国化学家道尔顿提出了原子是构成物质的基本粒子,它们是不可分割的实心球体1897年,英国科学家汤姆生在原子中发现了更小的粒子—电子
α粒子束发生偏转示意图α粒子束α粒子散射实验根据α粒子的运动情况初步探究原子的构成现象结论大多数α粒子能穿透金箔,而不改变原来的运动方向
一小部分α粒子改变了原来的运动方向
极少数α粒子被弹了回来
金箔原子内存在大量空间少数α粒子受到带电的粒子的作用原子内有质量大、体积小的核看课本第53页解决以下问题•1原子由哪两部分构成
•2原子核由什么构成
•3质子、中子、电子的电性和电量怎样
•4原子为什么不显电性
一、原子的构成原子电子原子核质子中子(带正电)(不带电)(带负电)(带正电)(不带电)核