高考化学一轮复习难溶电解质的溶解平衡跟踪检测及答案跟踪检测(二十八)难溶电解质的溶解平衡1.(2018·荆州模拟)已知一定量Ca(OH)2固体溶于水后,存在以下平衡状态:Ca(OH)2(s)Ca2+(aq)+2OH-(aq),Ksp=4
7×10-6,下列措施可使Ksp增大的是()A.升高温度B.降低温度C.加入适量CaO固体D.加入适量Na2CO3固体解析:选BKsp只与难溶电解质的性质和温度有关,而大多数难溶电解质的Ksp随温度的升高而增大,也有少数难溶电解质如Ca(OH)2,其Ksp随温度的升高而降低
2.某温度下,难溶物FeR的水溶液中存在平衡:FeR(s)Fe2+(aq)+R2-(aq),其沉淀溶解平衡曲线如图所示
下列说法正确的是()A.可以通过升温实现由a点变到c点B.b点对应的Ksp等于a点对应的KspC.d点可能有沉淀生成D.该温度下,Ksp=4×10-18解析:选B升高温度,FeR溶液中Fe2+和R2-的浓度同时增大,A项错误;沉淀溶解平衡曲线上的点均为平衡点,温度不变,Ksp不变,B项正确;d点相对于平衡点a点,c(Fe2+)相同,c(R2-)小于a点,没有沉淀生成,C项错误;选a点或b点计算,得Ksp(FeR)=2×10-18,D项错误
3.(2018·天津五区县期中)下列说法中正确的是()A.用等体积的蒸馏水或0
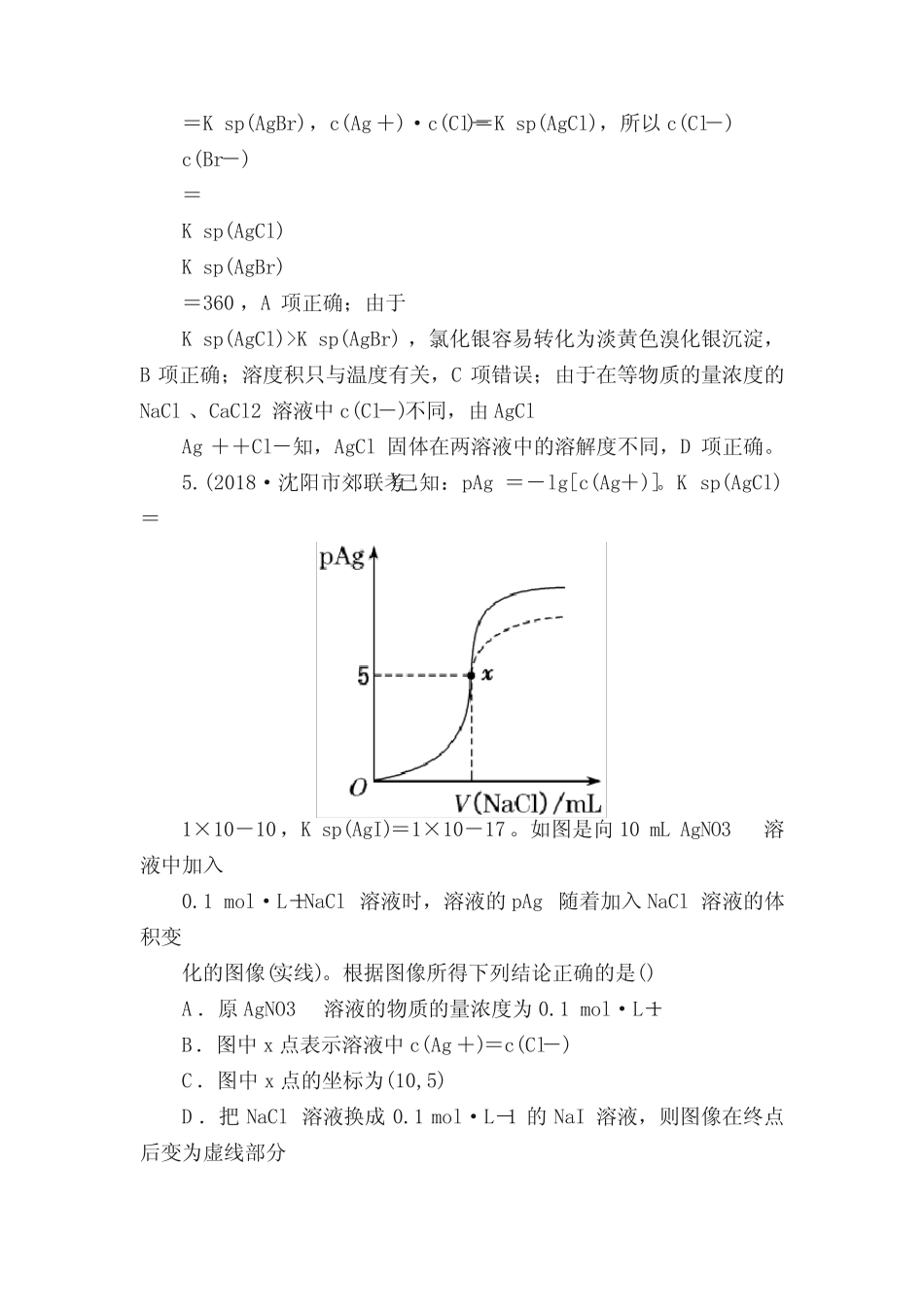
01mol·L-1盐酸洗涤AgCl沉淀,AgCl损失量相同B.向MgCO3沉淀中滴加NaOH溶液可以得到Mg(OH)2沉淀C.向氨水中加入NH4Cl或NaOH固体,溶液的pH均增大D.盐溶液加水稀释时,c(H+)、c(OH-)均减小解析:选BAgCl沉淀在水中存在溶解平衡:AgCl(s)Ag+(aq)+Cl-(aq),用盐酸洗涤时,c(Cl-)较大,使平衡逆向移动,AgCl的溶解度减小,故用蒸馏水洗涤AgCl时损失量比用盐酸洗涤AgCl时