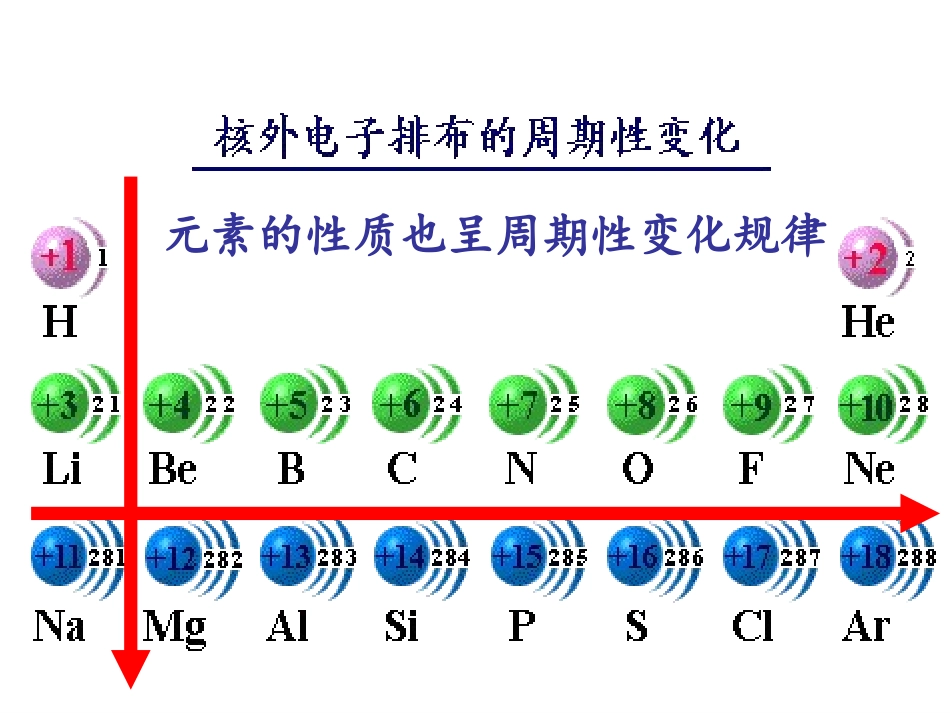
高三一轮复习——元素周期律及应用高三化学备课组吴双题组训练题组训练链接高考知识归纳元素的性质也呈周期性变化规律题组训练一——微粒半径大小的比较同周期元素(稀有气体除外)的原子,半径随核电荷数增大而逐渐减小
同主族元素的原子或离子,半径随核电荷数增大而逐渐增大(1)Na________Mg_______AlP______S______Cl电子层结构相同(核外电子排布相同)的离子(包括阳离子、阴离子),半径随核电荷数的增大而减小
同种元素形成的微粒半径,阳离子A>BB变式训练例2.(2011·重庆高考改编)1~20号元素中,下列叙述正确的是()A
元素最高正化合价与其主族序数相等B
非金属元素的最高正化合价与其负化合价的绝对值之和为8C
随着元素原子序数的递增,元素的最高正价从+1到+7,负价从-7到-1重复出现D.NaH中氢元素的化合价为-1题组训练二——元素化合价递变规律元素化合价递变规律①1~20号元素中,除了O、F外,主族元素的最高正价=主族序数=最外层电子数;最高正价+最低负价的绝对值=8②F无正价,O无最高正价③金属元素无负价(除零价外,在化学反应中只显正价);既有正价又有负价的元素一定是非金属元素;D如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是()A.原子半径:Z>Y>XB.WX3和水反应形成的化合物是离子化合物C.Y和Z两者最高价氧化物对应的水化物能相互反应D.气态氢化物的稳定性:RHI例3、写出相关化学式并进行比较例4、X、Y是元素周期表中ⅦA族中的两种元素,下列事实不能作为实验判据说明X的非金属性比Y强的是()A.单质的氧化性:X2>Y2B.Y的单质能将X从NaX的溶液中置换出来C.X的单质与H2化合更容易D.还原性:X—Z>Y>XB
最高价氧化物对应水化物的酸性:X>W>ZC
最简单气态氢化物的热稳定性:Y>X>W>ZD
元素X、Z、W的