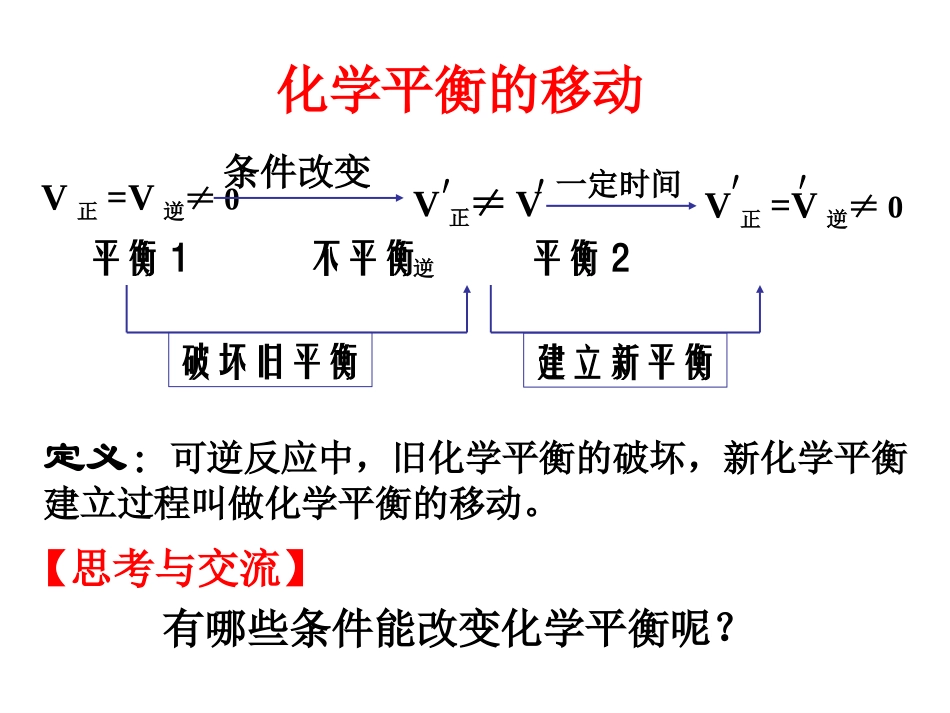
化学平衡的移动-定义:可逆反应中,旧化学平衡的破坏,新化学平衡建立过程叫做化学平衡的移动
V正≠V逆V正=V逆≠0条件改变平衡1不平衡平衡2建立新平衡破坏旧平衡V正=V逆≠0′′一定时间化学平衡的移动′′【思考与交流】有哪些条件能改变化学平衡呢
在其他条件不变时,增大反应物或减小生成物的浓度化学平衡向正反应方向移动减小反应物或增大生成物的浓度化学平衡向逆反应方向移动向右移动向左移动原因分析:1、运用浓度对化学反应速率的影响以及化学平衡的建立等知识,解释浓度对化学平衡的影响2、运用平衡常数知识解释浓度对化学平衡的影响1、浓度对化学平衡的影响1、已知在氨水中存在下列平衡:NH3+H2ONH3·H2ONH4++OH-(1)向氨水中加入MgCl2固体,平衡向移动,OH-浓度,NH4+浓度
(2)向氨水中加入浓盐酸,平衡向移动,此时溶液中浓度减小的粒子有
(3)向氨水中加入少量NaOH固体,平衡向
移动,此时发生的现象是
正反应方向减小增大正反应方向OH-、NH3·H2O、NH3逆反应方向有气体放出2、可逆反应C(s)+H2O(g)CO(g)+H2(g)在一定条件下达到平衡状态,改变下列条件,能否引起平衡移动
CO的浓度有何变化
①增大水蒸气浓度②加入更多的碳③增加H2浓度平衡正向移动,CO浓度增大平衡不移动,CO浓度不变平衡逆向移动,CO浓度减小解析:增加固体或纯液体的量不能改变其浓度,也不能改变速率,所以V(正)仍等于V(逆),平衡不移动
3、已知氯水中存在如下平衡:Cl2+H2OHCl+HClO
常温下,在一个体积为50mL的针筒内吸入40mL氯气后,再吸入10mL的水
写出针筒中可能观察到的现象
若将此针筒长时间放置在阳光下,又可以看到何种变化
试用平衡的观点加以解释
气体体积缩小,溶液呈浅黄绿色
气体体积继续减小,气体和溶液均变成无色
因为氯水中存在平衡:Cl2+H2OHC