第三节物质的实验制备[高考备考指南]考纲定位1
掌握常见气体的实验室制法(包括所用试剂、仪器、反应原理和收集方法)
涉及气体性质的实验探究和绿色化学理念
根据实验目的和要求,做到:①正确选用实验装置;②掌握控制实验条件的方法;③预测或描述实验现象
实验探究——能依据探究目的(物质的制备)设计并优化实验方案或实验装置,与同学交流实验探究的成果,提出进一步探究或改进实验的设想
社会责任——认识环境保护,注意绿色化学观念,防止尾气污染空气
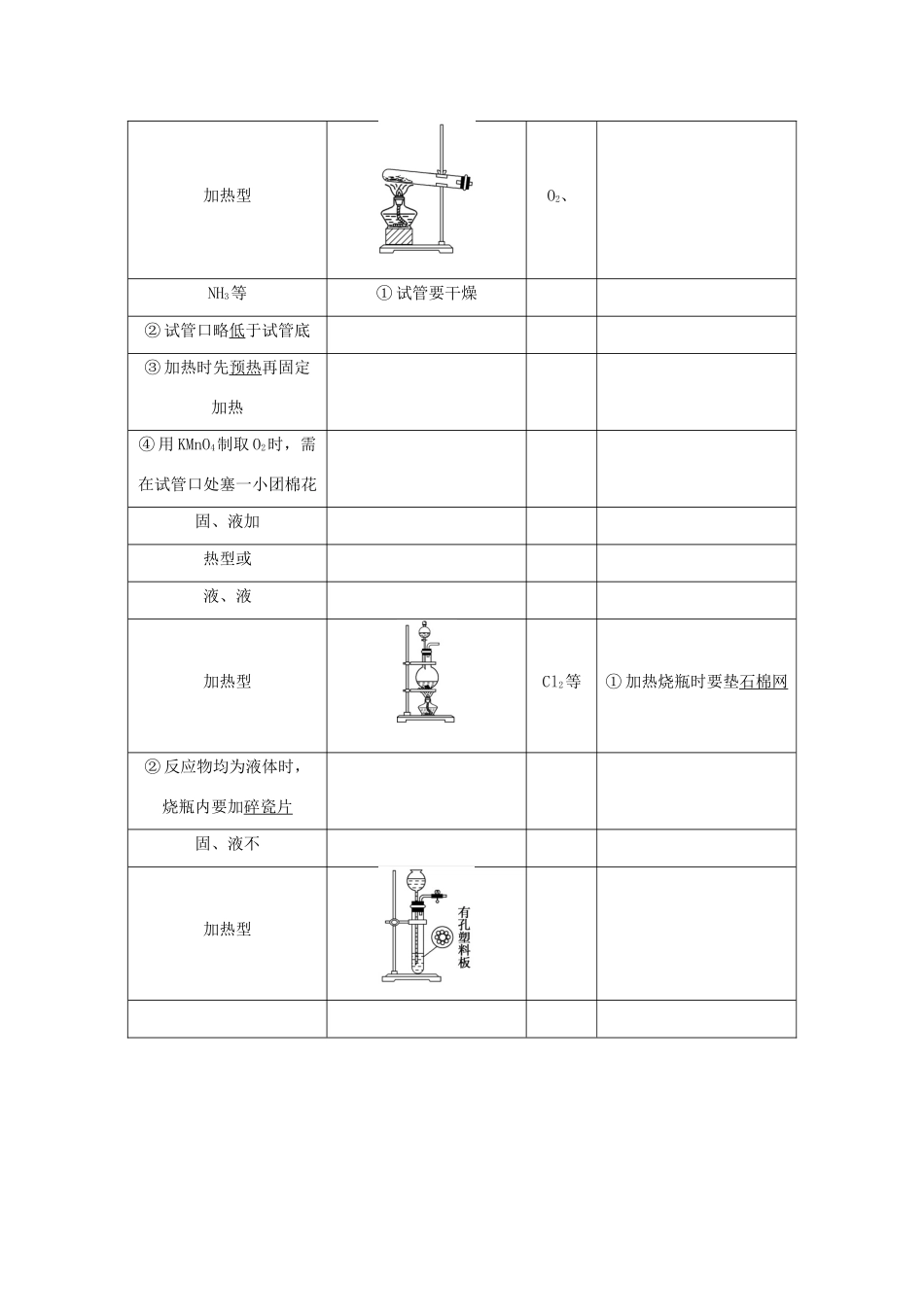
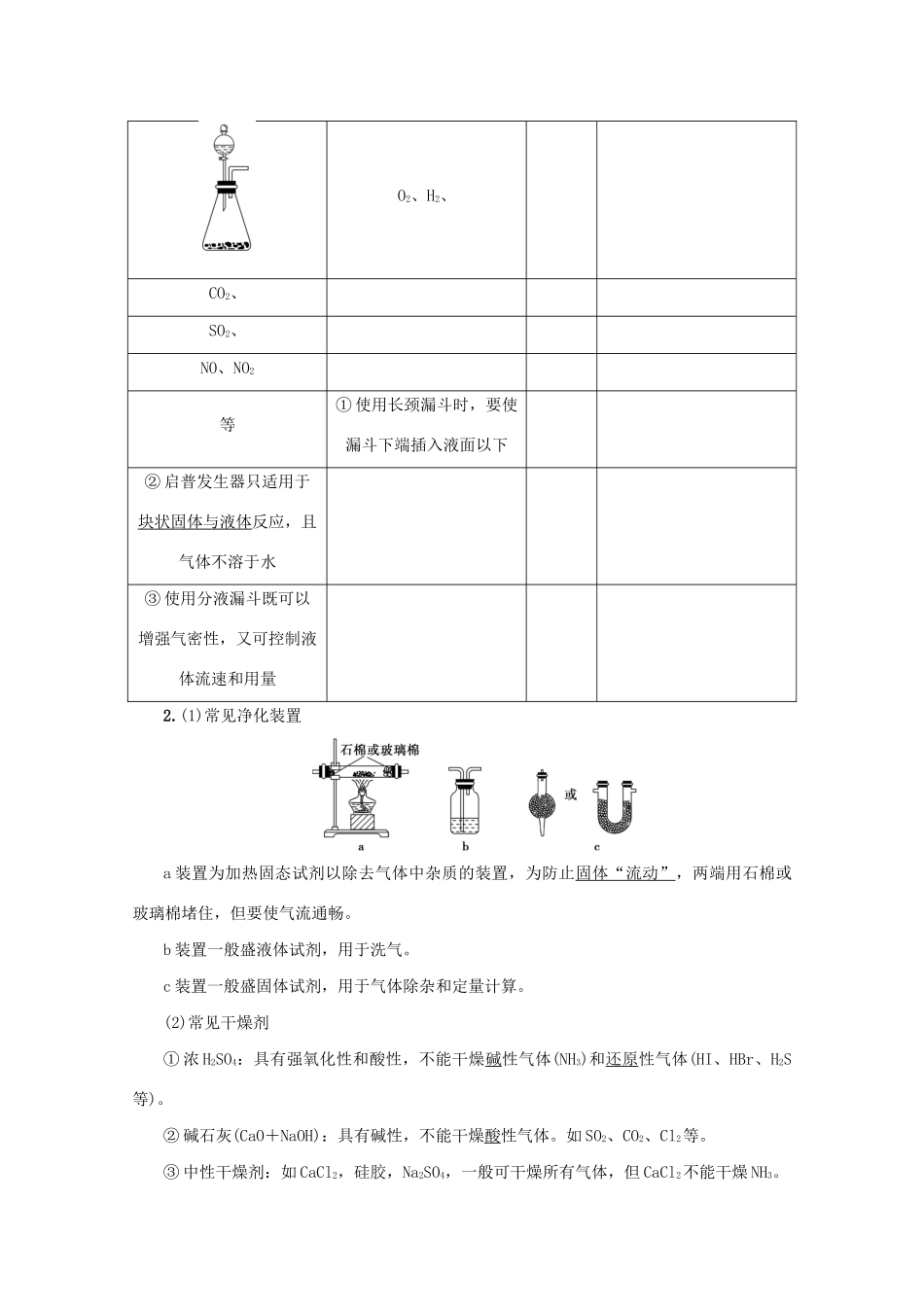
常见气体的制备(对应复习讲义第126页)1.常见气体制备的发生装置选择发生装置一般需从反应物的状态、溶解性和反应条件确定制气装置类型,具体如下表中所示:装置类型装置图适用气体操作注意事项固、固加热型O2、NH3等①试管要干燥②试管口略低于试管底③加热时先预热再固定加热④用KMnO4制取O2时,需在试管口处塞一小团棉花固、液加热型或液、液加热型Cl2等①加热烧瓶时要垫石棉网②反应物均为液体时,烧瓶内要加碎瓷片固、液不加热型O2、H2、CO2、SO2、NO、NO2等①使用长颈漏斗时,要使漏斗下端插入液面以下②启普发生器只适用于块状固体与液体反应,且气体不溶于水③使用分液漏斗既可以增强气密性,又可控制液体流速和用量2
(1)常见净化装置a装置为加热固态试剂以除去气体中杂质的装置,为防止固体“流动”,两端用石棉或玻璃棉堵住,但要使气流通畅
b装置一般盛液体试剂,用于洗气
c装置一般盛固体试剂,用于气体除杂和定量计算
(2)常见干燥剂①浓H2SO4:具有强氧化性和酸性,不能干燥碱性气体(NH3)和还原性气体(HI、HBr、H2S等)
②碱石灰(CaO+NaOH):具有碱性,不能干燥酸性气体
如SO2、CO2、Cl2等
③中性干燥剂:如CaCl2,硅胶,Na2SO4,一般可干燥所有气体,但CaCl2不能干燥NH3
3.常见气体的收集