硫酸硝酸和氨(第2课时)教学目的:1、掌握硝酸的化学性质
2、利用实验,使学生掌握硝酸的特性——强氧化性;通过讨论、分析、对比的方式,使学生掌握浓硝酸的氧化性大于稀硝酸的氧化性;利用分析演绎的方式,使学生掌握硝酸与碳的反应
3、通过硝酸跟硫酸的对比和分析,对学生进行辩证唯物主义教育
教学重点、难点重点:硝酸的氧化性难点:硝酸的氧化性教学环节教师活动学生活动新课导入铜在金属活动性顺序表中位于氢之后,而能被浓H2SO4氧化,那么在氢之前的金属是否更容易被其氧化呢
新知学习活动探究①将一根随时处理完氧化膜的铝条迅速置于盛饱和CuSO4溶液的试管中,过一会儿取出
(可用热NaOH溶液处理氧化膜,)②把铝条表面的铜用砂纸打掉洗净后,将其插入盛浓H2SO4的试管中,1~2分钟后取出
③把②中的铝条放入饱和CuSO4溶液中,过一会儿取出
④把③中铝条取出,置于浓H2SO4中,加热
观察实验现象,并思考原因学习探究1、根据实验①的现象,写出化学反应方程式2、洁净铝条置于浓H2SO4中无明显现象,难道不反应吗
3、①③对比,现象不同,说明在②中一定发生了某种反应
根据铝的性质,推测发生了什么反应
该过程体现浓硫酸的什么性质
4、实验④说明了什么问题
2Al+3Cu2+==2Al3++3Cu学生联想到Al2O3保护膜的作用思考总结浓硫酸与金属反应的特征用心爱心专心归纳整理A、加热条件下,浓H2SO4可氧化大多数金属(Au、Pt等除外),但不产生H2
B、常温下,浓H2SO4可使Fe、Al钝化
C、浓H2SO4与金属反应表现酸性和氧化性
D、“钝化”并非不反应,是因氧化而钝化
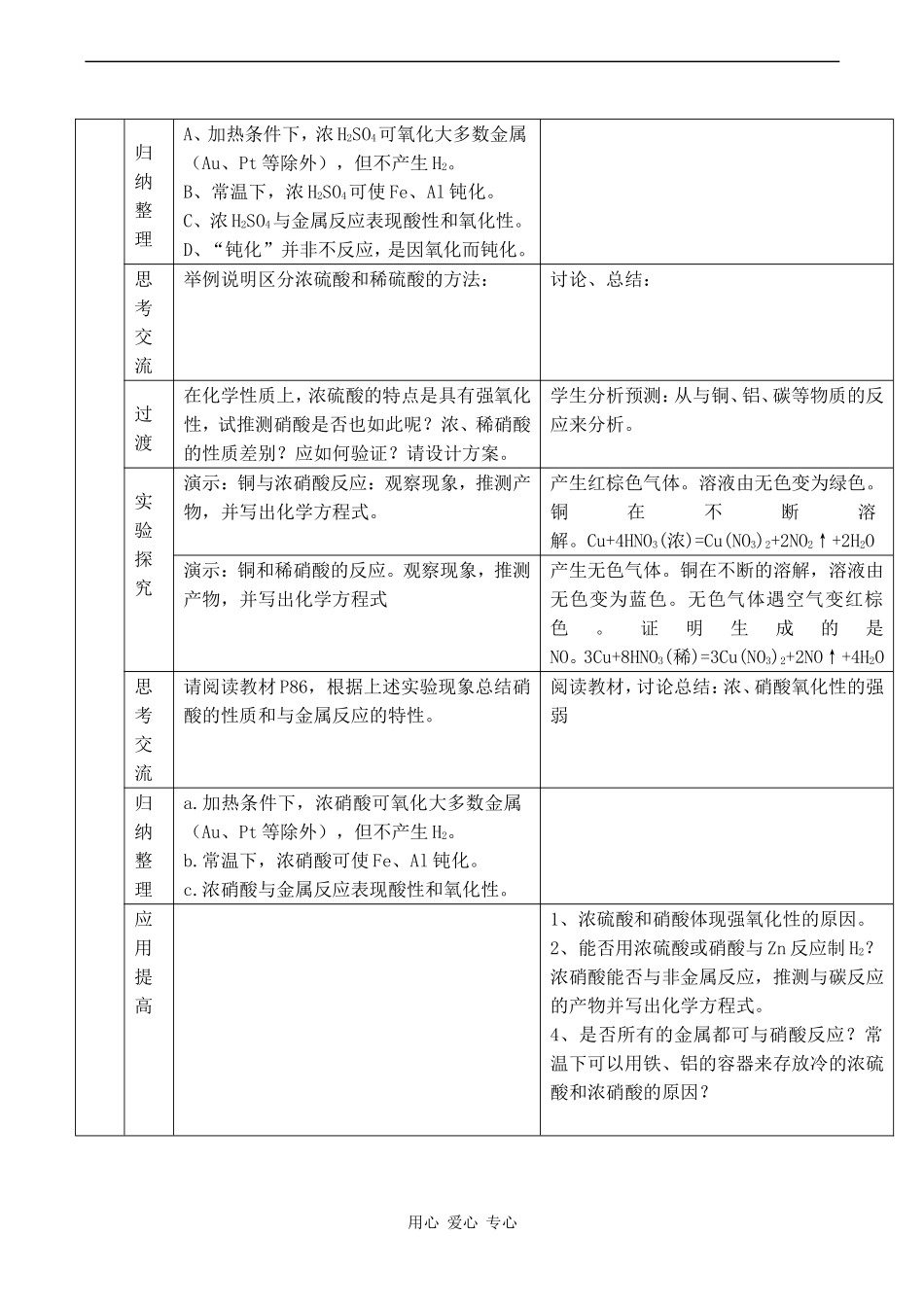
思考交流举例说明区分浓硫酸和稀硫酸的方法:讨论、总结:过渡在化学性质上,浓硫酸的特点是具有强氧化性,试推测硝酸是否也如此呢
浓、稀硝酸的性质差别
学生分析预测:从与铜、铝、碳等物质的反应来分析