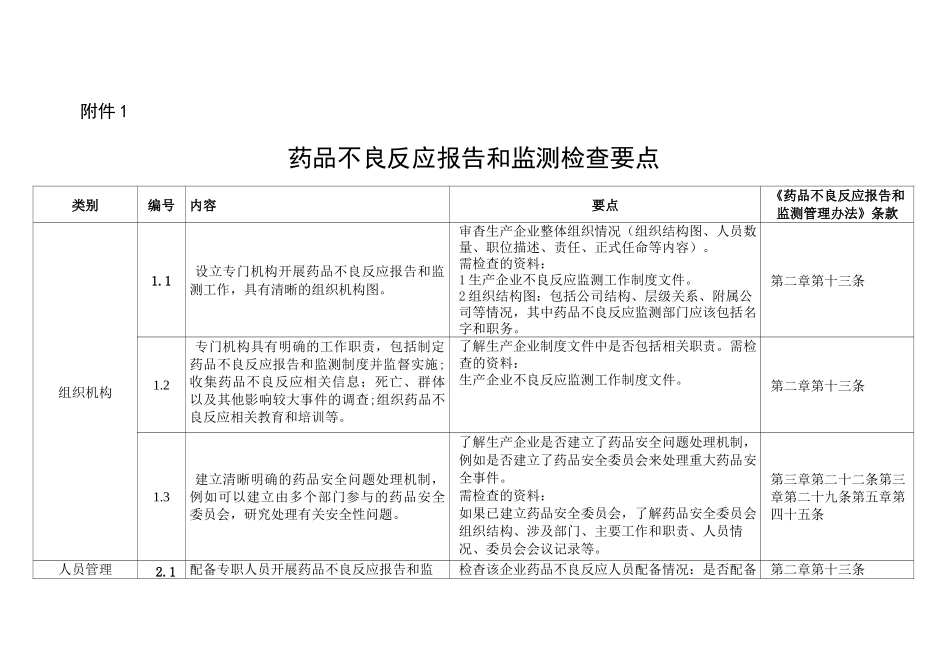
附件1药品不良反应报告和监测检查要点类别编号内容要点《药品不良反应报告和监测管理办法》条款组织机构1
1设立专门机构开展药品不良反应报告和监测工作,具有清晰的组织机构图
审杳生产企业整体组织情况(组织结构图、人员数量、职位描述、责任、正式任命等内容)
需检查的资料:1生产企业不良反应监测工作制度文件
2组织结构图:包括公司结构、层级关系、附属公司等情况,其中药品不良反应监测部门应该包括名字和职务
第二章第十三条1
2专门机构具有明确的工作职责,包括制定药品不良反应报告和监测制度并监督实施;收集药品不良反应相关信息;死亡、群体以及其他影响较大事件的调查;组织药品不良反应相关教育和培训等
了解生产企业制度文件中是否包括相关职责
需检查的资料:生产企业不良反应监测工作制度文件
第二章第十三条1
3建立清晰明确的药品安全问题处理机制,例如可以建立由多个部门参与的药品安全委员会,研究处理有关安全性问题
了解生产企业是否建立了药品安全问题处理机制,例如是否建立了药品安全委员会来处理重大药品安全事件
需检查的资料:如果已建立药品安全委员会,了解药品安全委员会组织结构、涉及部门、主要工作和职责、人员情况、委员会会议记录等
第三章第二十二条第三章第二十九条第五章第四十五条人员管理2
1配备专职人员开展药品不良反应报告和监检杳该企业药品不良反应人员配备情况:是否配备第二章第十三条类别编号内容要点《药品不良反应报告和监测管理办法》条款测工作
药品不良反应监测联系人(本企业药品不良反应监测总负责人)、药品不良反应部门负责人,专职药品不良反应工作人员、市场等部门的药品不良反应监测员等
需检查的资料:药品不良反应部门负责人、药品不良反应专职工作人员、其他部门药品不良反应信息员有关资料,包括聘任时间、资质条件、工作职责、联系方式等
2药品不良反应监测部门工作人员具有明确的工作职责,包括收集、核实、分