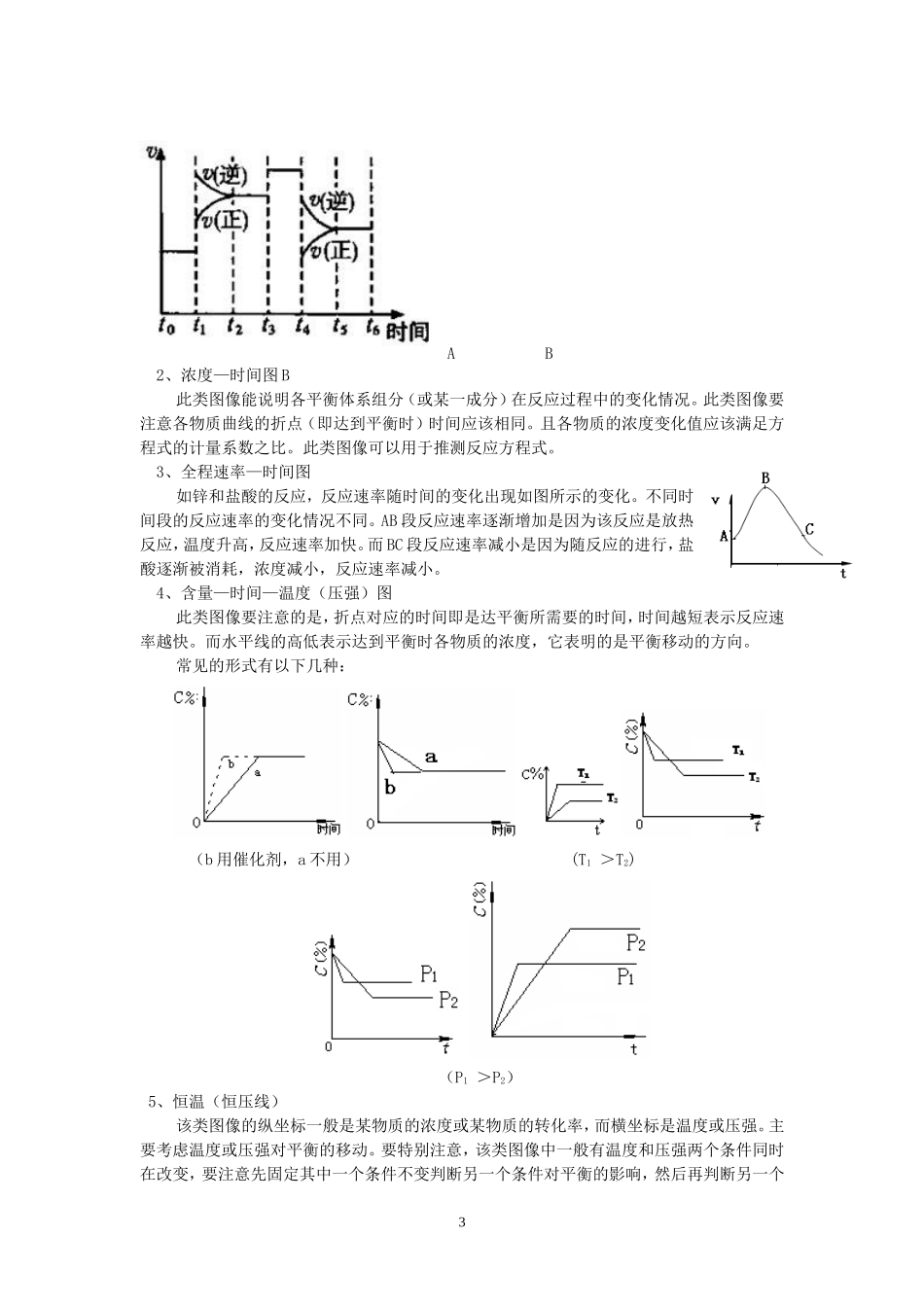
1第四部分化学反应原理第一章化学反应与能量一、热化学方程式及盖斯定律:1.热化学方程式的书写要注意标明各物质的状态,方程式系数可以是分数或小数。2.不管化学反应是一步完成或分几步完成,其反应热是相同的。化学反应的焓变(ΔH)只与反应体系的始态和终态有关,而与反应的途径无关。3.有关利用盖斯定律的计算,合理设计反应途径,正确加减热化学方程式及其ΔH求得未知热化学方程式及ΔH。4.热化学方程式的意义:热化学方程式:S(s)+O2(g)SO2(g)△H=-296KJ/mol,的意义是:32g硫粉完全燃烧生成二氧化硫气体,放出296kJ的热量二、(1)燃烧热:在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量。(2)中和热:在稀溶液中,酸和碱发生中和反应生成1mol水时的反应热。三、反应热的计算(1)由化学反应的实质可知,一个给定反应的反应热可利用反应物和生成物的键能来计算。ΔH=Σ反应物的键能-Σ生成物的键能(2)由反应热与物质能量的关系可知,一个给定反应的反应热可利用反应物和生成物的能量来计算。ΔH=Σ生成物的能量-Σ反应物的能量由于物质的能量取决于物质的性质和测定时的温度和压强,因此一个给定反应的反应热仅与反应的始态和终态有关,而与反应完成的途径无关——盖斯定律。第二章化学反应速率与化学平衡第一单元化学反应速率一、化学反应速率计算公式:单位:mol·L-1·s-1或mol·L-1·min-1说明:同一反应中,各物质速率之比等于系数之比。㈡、外界条件对化学反应速率的影响影响因素影响结果(其他条件不变的前提下)C增大反应物的浓度,可以增大反应速率;减小反应物的浓度,可以减小化学反应的速率。(适用于气体或溶液的反应)P对于有气体参加的反应,若其他条件不变,增大压强,反应速率加快;减小压强,反应速率减慢。(适用于有气体参加的反应)T升高温度,可以增大反应速率,降低温度,可以减慢反应速率催化剂催化剂可以改变化学反应的速率。正催化剂:能够加快反应速率的催化剂。其他:表面积块状固体:粉碎。液体:喷洒雾化第二单元化学反应的方向和限度一、化学平衡1.化学平衡状态的标志(1)υ正=υ逆(本质特征)(2)反应混合物中各组成成分的浓度保持不变二.化学平衡常数2对于反应:nA(g)+mB(g)pC(g)+qD(g),K=(固体和纯液体不列入表达式)。浓度积:Q=Q〈K:反应向正反应方向进行;Q=K:反应处于平衡状态;Q〉K:反应向逆反应方向进行注意:①用浓度列三段式求平衡常数。②K有单位,其单位与表达式有关;③K表示反应进行的程度,K越大,进行的程度越大;其值只与温度有关,如正反应放热,温度升高,平衡逆向移动,K值减小。④方程式相加,K相乘;方程式相减,K相除;方程式相反,K为倒数。第三单元化学平衡的移动一、化学平衡的移动(1)定义:可逆反应中旧的化学平衡的破坏,新化学平衡的建立过程叫化学平衡的移动。(2)移动的原因:外界条件发生变化。移动的方向:由v正和v逆的相对大小决定。二、影响化学平衡的条件1、速率—时间图A此类图像定性地揭示了正、逆反应速率随时间(含条件变化对速率的影响)而变化的规律,体现了平衡的“逆、等、动、定、变、同”的基本特征,以及平衡移动的方向等。旧平衡新平衡①若V正>V逆,平衡不移动。②若V正=V逆,③若V正<V逆,平衡向逆反应方向移动平衡向正反应方向移动。条件改变一段时间后v正≠v逆3AB2、浓度—时间图B此类图像能说明各平衡体系组分(或某一成分)在反应过程中的变化情况。此类图像要注意各物质曲线的折点(即达到平衡时)时间应该相同。且各物质的浓度变化值应该满足方程式的计量系数之比。此类图像可以用于推测反应方程式。3、全程速率—时间图如锌和盐酸的反应,反应速率随时间的变化出现如图所示的变化。不同时间段的反应速率的变化情况不同。AB段反应速率逐渐增加是因为该反应是放热反应,温度升高,反应速率加快。而BC段反应速率减小是因为随反应的进行,盐酸逐渐被消耗,浓度减小,反应速率减小。4、含量—时间—温度(压强)图此类图像要注意的是,折点对应的时间即是达平衡所需要的时间,时间越短表示反应速率越快。而水平线的高低表示达到平衡时各物质的浓度,...